
某課題組以苯為主要原料,采用以下路線合成利膽藥——柳胺酚
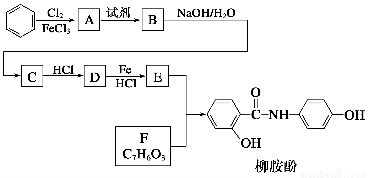
已知:
回答下列問題:
(1)對于柳胺酚,下列說法正確的是________。
A.1 mol柳胺酚最多可以和2 mol NaOH反應
B.不發(fā)生硝化反應
C.可發(fā)生水解反應
D.可與溴發(fā)生取代反應
(2)寫出A→B反應所需的試劑________。
(3)寫出B→C的化學方程式________________________________。
(4)寫出化合物F的結構簡式__________。
(5)寫出同時符合下列條件的F的同分異構體的結構簡式________________
________________________________________(寫出3種)。
①屬酚類化合物,且苯環(huán)上有三種不同化學環(huán)境的氫原子。
②能發(fā)生銀鏡反應。
(6)以苯和乙烯為原料可合成聚苯乙烯,請設計合成路線(無機試劑及溶劑任選)
注:合成路線的書寫格式參照如下示例流程圖:
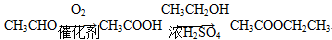
 津橋教育計算小狀元系列答案
津橋教育計算小狀元系列答案科目:高中化學 來源:2013-2014學年高考化學二輪復習四川配套訓練 第5講化學反應與能量練習卷(解析版) 題型:選擇題
為保護環(huán)境并緩解能源危機,專家提出利用太陽能促使燃燒循環(huán)使用的構想,轉化關系如圖所示。
已知:

(1)過程Ⅰ可用如下反應表示:①2CO2 2CO+O2
2CO+O2
②2H2O(g)  2H2+O2
2H2+O2
③2N2+6H2O 4NH3+3O2
4NH3+3O2
④2CO2+4H2O 2CH3OH+3O2
2CH3OH+3O2
⑤2CO+4H2O ________+3O2。
________+3O2。
(2)25 ℃時,a g CH4完全燃燒釋放出b kJ熱量。下列說法不正確的是( )。
A.過程Ⅰ是將太陽能轉化成化學能
B.反應⑤的另一種產(chǎn)物為CH4
C.ΔH1=-ΔH2
D.表示甲烷燃燒熱的熱化學反應方程式為CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-16b kJ·mol-1
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習四川配套訓練 第1講物質組成性質分類練習卷(解析版) 題型:填空題
下面是有關物質的轉化關系圖,其中A為單質,E在常溫下為液體,D是一種溫室氣體,C的相對分子質量為78。請回答相關問題。

(1)下列對C的結構、性質推斷中不正確的是( )。
A.久置于空氣中會變成白色
B.具有強氧化性
C.晶體中存在離子鍵與非極性鍵
D.是一種堿性氧化物
(2)A的原子結構示意圖為______________,H的電子式為______________,E的結構式為____________________。
(3)C和E反應生成H的離子方程式為__________________,反應中氧化劑與還原劑的物質的量之比為______。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習四川配套訓練 第12講化學實驗基礎練習卷(解析版) 題型:填空題
某種粗鹽中含有泥沙、Ca2+、Mg2+、Fe3+、SO等雜質。某同學在實驗室中設計了用這種粗鹽制備精鹽的方案如下(用于沉淀的試劑稍過量):

請回答以下問題:
(1)為操作Ⅳ選擇所需儀器(用標號字母填寫):________。
A.燒杯 B.試管 C.玻璃棒 D.分液漏斗 E.漏斗 F.酒精燈
G.蒸發(fā)皿
(2)操作Ⅲ中常用Na2CO3溶液、NaOH溶液、BaCl2溶液作為除雜試劑,則加入除雜試劑的順序為:NaOH溶液→________→________。
(3)操作Ⅲ中,判斷加入BaCl2已過量的方法是___________________________________
(4)操作Ⅴ應選擇的酸是________,若將操作Ⅴ與操作Ⅳ的先后順序對調,將會對實驗結果產(chǎn)生的影響是___________________________________
(5)操作Ⅵ是________(選擇合理操作的名稱,用標號字母按操作先后順序填寫)。
a.過濾、洗滌 B.蒸發(fā)、濃縮 c.萃取、分液 D.冷卻、結晶
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習四川配套訓練 第12講化學實驗基礎練習卷(解析版) 題型:選擇題
為提純下列物質(括號內的物質是雜質)所選用的除雜試劑和分離方法都正確的是( )。
被提純的物質除雜試劑分離方法
A溴化鈉溶液(NaI)新制氯水、CCl4萃取、分液
B氯化銨溶液(FeCl3)氫氧化鈉溶液過濾
C二氧化碳(CO)氧化銅粉末通過灼熱的氧化銅粉末
D碳酸鈉(偏鋁酸鈉)鹽酸過濾
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習四川配套訓練 第10講金屬元素化合物練習卷(解析版) 題型:填空題
銀銅合金廣泛用于航空工業(yè),從切割廢料中回收銀并制備銅化工產(chǎn)品的工藝如下:

(注:Al(OH)3和Cu(OH)2開始分解的溫度分別為450 ℃和80 ℃。)
(1)電解精煉銀時,陰極反應式為________;濾渣A與稀HNO3反應,產(chǎn)生的氣體在空氣中迅速變?yōu)榧t棕色,該氣體變色的化學反應方程式為________________。
(2)固體混合物B的組成為__________;在生成固體B的過程中,需控制NaOH的加入量,若NaOH過量,則因過量引起的反應的離子方程式為____________。
(3)完成煅燒過程中一個反應的化學方程式:
CuO+____Al2O3 ____CuAlO2+________↑。
____CuAlO2+________↑。
(4)若銀銅合金中銅的質量分數(shù)為63.5%,理論上5.0 kg廢料中的銅可完全轉化為________ mol CuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液________ L。
(5)CuSO4溶液也可用于制備膽礬,其基本操作是________、過濾、洗滌和干燥。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習四川配套訓練 第10講金屬元素化合物練習卷(解析版) 題型:選擇題
已知A是一種金屬單質,B顯淡黃色,其轉化關系如圖所示,則C的以下性質錯誤的是( )。

A.溶液呈堿性
B.與澄清石灰水反應產(chǎn)生白色沉淀
C.與足量鹽酸反應放出氣體
D.受熱易分解
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習 專題8電化學原理練習卷(解析版) 題型:填空題
電解是最強有力的氧化還原手段,在化工生產(chǎn)中有著重要的應用。請回答下列問題:
(1)以銅為陽極,以石墨為陰極,用NaCl溶液作電解液進行電解,得到半導體材料Cu2O和一種清潔能源,則陽極反應式為__________________,陰極反應式為________。
(2)某同學設計如圖所示的裝置探究金屬的腐蝕情況。下列判斷合理的是____________(填序號)。

a.②區(qū)銅片上有氣泡產(chǎn)生
b.③區(qū)鐵片的電極反應式為2Cl--2e-===Cl2↑
c.最先觀察到變成紅色的區(qū)域是②區(qū)
d.②區(qū)和④區(qū)中銅片的質量均不發(fā)生變化
(3)最新研究發(fā)現(xiàn),用隔膜電解法處理高濃度乙醛廢水的工藝具有流程簡單、能耗較低等優(yōu)點,其原理是使乙醛分別在陰、陽極發(fā)生反應生成乙醇和乙酸,總反應式為2CH3CHO+H2O CH3CH2OH+CH3COOH
CH3CH2OH+CH3COOH
實驗室中,以一定濃度的乙醛?Na2SO4溶液為電解質溶液,模擬乙醛廢水的處理過程,其裝置如圖所示。

①若以甲烷堿性燃料電池為直流電源,則燃料電池中b極應通入__________(填化學式),電極反應式為____________________。電解過程中,陰極區(qū)Na2SO4的物質的量________(填“增大”、“減小”或“不變”)。
②在實際工藝處理中,陰極區(qū)乙醛的去除率可達60%。若在兩極區(qū)分別注入1 m3乙醛含量為3 000 mg·L-1的廢水,可得到乙醇________kg(計算結果保留小數(shù)點后一位)。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習 專題5化學反應與能量變化練習卷(解析版) 題型:選擇題
工業(yè)生產(chǎn)硫酸過程中,SO2在接觸室中被催化氧化為SO3,已知該反應為放熱反應。現(xiàn)將2 mol SO2、1 mol O2充入一密閉容器充分反應后,放出熱量98.3 kJ,此時測得SO2的轉化率為50%。下列熱化學方程式正確的是( )。
A.2SO3(g) 2SO2(g)+O2(g) ΔH=+196.6 kJ·mol-1
2SO2(g)+O2(g) ΔH=+196.6 kJ·mol-1
B.2SO2(g)+O2(g) SO3(g) ΔH=-98.3 kJ·mol-1
SO3(g) ΔH=-98.3 kJ·mol-1
C.SO2(g)+ O2(g)
O2(g) SO3(g) ΔH=+98.3 kJ·mol-1
SO3(g) ΔH=+98.3 kJ·mol-1
D.SO2(g)+ O2(g)
O2(g) SO3(g) ΔH=-196.6 kJ·mol-1
SO3(g) ΔH=-196.6 kJ·mol-1
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com