
(1)在NaCl、NaOH、Na2O2、N2、H2S、H2O2中, 只含有離子鍵的是 ,只含有極性鍵的是 ,只含有非極性鍵的是 ,既含有離子鍵又含有極性鍵的是 ,既含有離子鍵又含有非極性鍵的是 。
(2)用電子式表示下列物質的形成過程:
MgCl2 (2分)
H2O (2分)
 期末100分闖關海淀考王系列答案
期末100分闖關海淀考王系列答案 小學能力測試卷系列答案
小學能力測試卷系列答案科目:高中化學 來源: 題型:閱讀理解
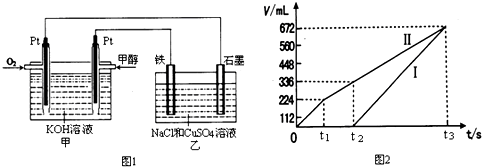
| 容器 | A | B |
| 反應物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
| CH3OH(g)濃度(mol?L-1) | c1 | c2 |
| 反應能量變化 | 放出29.4kJ | 吸收akJ |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 (2013?河西區一模)肼(N2H4)和氨是氮的兩種常見化合物,在科學技術和生產中有廣泛應用.請按要求回答下列問題:
(2013?河西區一模)肼(N2H4)和氨是氮的兩種常見化合物,在科學技術和生產中有廣泛應用.請按要求回答下列問題:

| ||
| ||
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
| n(NH3) |
| n(CO2) |
| n(N2) | n(H2) | n(NH3) | |
| 甲 | 1mol | 3mol | 0mol |
| 乙 | 0.5mol | 1.5mol | 1mol |
| 丙 | 0mol | 0mol | 4mol |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
如圖,直線交點處的圓圈為NaCl晶體中Na+和Cl-所處的位置。這兩種離子在空間三個互相垂直的方向上都是等距離排列的。
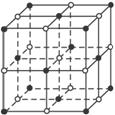
(1)請將其中代表Na+的圓圈涂黑(不考慮體積大小),以完成NaCl晶體結構示意圖。
(2)晶體中,在每個Na+周圍與它最接近的且距離相等的Na+共有( )
A.4個 B.6個 C.8個 D.12個
(3)晶體中,與每個Na+距離相等且距離最近的n個Cl-所圍成的空間幾何構型為( )
A.正四面體 B.正六面體
C.正八面體 D.正二十面體
(4)晶體中每一個重復的結構單元叫晶胞。在NaCl晶胞中正六面體的頂點上、面上、棱上的Na+或Cl-為該晶胞與其相鄰的晶胞所共有,一個晶胞中Cl-的個數等于________個,即________(填計算式),Na+的個數等于___________,即________________________________(填計算式)。
(5)設NaCl的摩爾質量為M g·mol-1,食鹽晶體的密度為ρ g·cm-3,阿伏加德羅常數為NA。食鹽晶體中兩個距離最近的Na+中心的距離為___________cm。
查看答案和解析>>
科目:高中化學 來源:2012屆浙江省紹興一中高三5月模擬考試理科綜合化學試卷(帶解析) 題型:填空題
(14分)已知A、B、C、D、E為中學化學常見的五種物質,均含元素R,R在A、B、C、D、E中所呈化合價依次遞增,其中只有B為單質。常溫下,A、B、C、D為氣體,且D+H2O→C+E。
請回答下列問題:
⑴元素R在元素周期表中的位置為_________ ____; B分子的電子式為__________。
⑵已知氣體D與NaOH溶液1:1恰好完全反應,生成R的兩種含氧酸鹽,所得溶液中各離子濃度大小關系 。
⑶將22.4L某R的氧化物與足量的灼熱銅粉完全反應后,氣體體積變為11.2L(體積均在相同條件下測定),則該氧化物的化學式可能為 。(填序號)
①、RO2 ②、R2O3 ③、RO ④、R2O
⑷科學家制備的另一種化合物,與A的組成元素相同,具有很高的熱值,可用作火箭和燃料電池的燃料。該化合物可由次氯酸鈉溶液和A反應得到,寫出該反應的化學方程式 。
⑸M為E的鈉鹽,一定條件下可發生如下反應:
①設計實驗方案,鑒定常見物質N 。
②此外,科學家還制備了另一種鈉鹽X,其與P的組成元素完全相同,X中的陰離子與P中的陰離子表觀形式相同(元素種類和原子個數均相同),但X中陰離子的結構中含有一個過氧鍵:-O-O- ,電導實驗表明,同條件下其電導能力與NaCl相同,鈉鹽X的陰離子與水反應生成過氧化氫的離子方程式為 。
| 25℃平衡體系(苯、水、HA) | 平衡常數 | 焓變 | 起始總濃度 |
在水中,HA H++A- H++A- | K1 | △H1 | 3.0×10-3 mol·L-1 |
在苯中,2HA (HA)2 (HA)2 | K2 | △H2 | 4.0×10-3 mol·L-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com