
分析 依據方程式:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,2Cl2+2Ca(OH)2═CaCl2+2H2O+Ca(ClO)2,可知MnO2~Cl2~0.5Ca(ClO)2,依據生成次氯酸鈣71.5g,計算二氧化錳的質量,最后依據$\frac{m(二氧化錳)}{m(軟錳礦)}$×100%計算軟錳礦中二氧化錳的質量分數.
解答 解:依據方程式:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,2Cl2+2Ca(OH)2═CaCl2+2H2O+Ca(ClO)2,濃鹽酸足量,軟錳礦中的二氧化錳完全反應,
則MnO2~Cl2~0.5Ca(ClO)2,
87g 0.5×143g
m 71.5g
87:m=(0.5×143g ):71.5g 解得m=87g,
軟錳礦中二氧化錳的質量分數=$\frac{m(二氧化錳)}{m(軟錳礦)}$×100%=$\frac{87g}{150g/mol}$×100%=58%;
答:軟錳礦中二氧化錳的質量分數是58%.
點評 本題考查根據方程式進行的有關計算,明確發生的化學反應,依據方程式找出二氧化錳與次氯酸鈣之間量的關系即可解答,題目難度不大.


 點睛新教材全能解讀系列答案
點睛新教材全能解讀系列答案 小學教材完全解讀系列答案
小學教材完全解讀系列答案科目:高中化學 來源: 題型:選擇題
| A. | Cu$\stackrel{H_{2}SO_{4}}{→}$Cu | B. | Cu$\stackrel{CuSO_{4}}{→}$Ag | C. | Zn$\stackrel{NH_{4}Cl}{→}$C | D. | Zn$\stackrel{C_{2}H_{5}OH}{→}$Cu |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
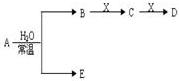 已知A、B、C、D、E、X存在如圖所示轉化關系(部分生成物和反應條件略去).
已知A、B、C、D、E、X存在如圖所示轉化關系(部分生成物和反應條件略去). .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
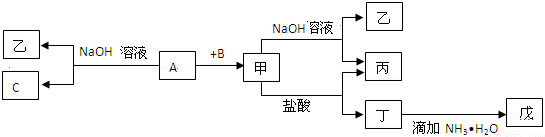
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
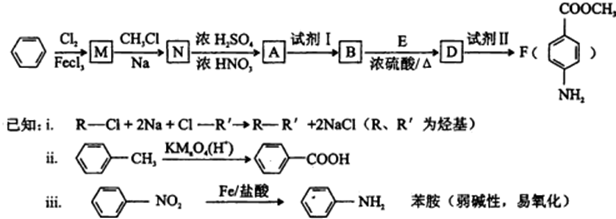
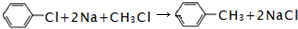 .
.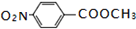 .
. ;
;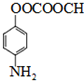 .
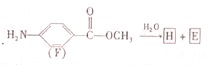
.
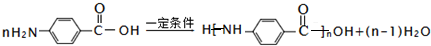 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2O2能與CO2反應,可用作呼吸面具的供氧劑 | |
| B. | 硅是半導體材料,可用于制備光導纖維 | |
| C. | 明礬能水解生成Al(OH)3膠體,可用作凈水劑 | |
| D. | Al2O3熔點高,可用于制作耐高溫儀器 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 蔗糖、淀粉、蛋白質、油脂都是營養物質,都屬于高分子化合物,都能發生水解反應 | |
| B. | 人造纖維、合成纖維、碳纖維、光導纖維主要成分都是纖維素 | |
| C. | 乙醇、乙酸、乙酸乙酯都能發生取代反應,乙酸乙酯中的少量乙酸可用飽和Na2CO3溶液除去 | |
| D. | 甲烷、乙烯和苯在工業上都可通過石油分餾得到 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 元素的原子半徑呈周期性變化 | |
| B. | 元素原子量的遞增,量變引起質變 | |
| C. | 元素的金屬性和非金屬性呈周期性變化 | |
| D. | 元素原子的核外電子排布呈周期性變化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com