
| A. | 4a+4b+4c | B. | 2a-2b+6c | C. | 2a-2b+2c | D. | 2a-6b+2c |
分析 92g液態酒精的物質的量為$\frac{92g}{46g/mol}$=2mol,根據蓋斯定律構造出目標熱化學反應方程式,
①C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g)△H1=-a kJ/mol
②C2H5OH(g)═C2H5OH(l)△H2=-b kJ/mol
③H2O(g)═H2O(l)△H3=-c kJ/mol
[①-②+③×3]得:C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)反應熱與化學計量數成正比,據此計算判斷.
解答 解:已知:①C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g)△H1=-a kJ/mol
②C2H5OH(g)═C2H5OH(l)△H2=-b kJ/mol
③H2O(g)═H2O(l)△H3=-c kJ/mol
由蓋斯定律[①-②+③×3]得:C2 H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)則△H=-(a-b+3c)kJ•mol-1,
92g液態酒精的物質的量為$\frac{92g}{46g/mol}$=2mol,完全燃燒,最后恢復到室溫,反應熱與化學計量數成正比,則放出的熱量(單位kJ)為2a-2b+6c,
故選B.
點評 本題考查根據蓋斯定律計算反應熱,題目難度不大,關鍵是構造目標熱化學反應方程式,注意反應熱的符號.


科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑:Z<Y<W,而離子半徑:W<Y<Z | |
| B. | 含W的鹽溶液一定呈酸性 | |
| C. | 由X、Y、Z組成的鹽的水溶液呈酸性,則溶液中該鹽陽離子濃度大于酸根離子濃度 | |
| D. | W和Y形成的原子個數比為1:1的共價化合物,具有耐高溫、抗沖擊、導熱性好等優良性質,被廣泛應用于電子工業、陶瓷工業等領域,是一種原子晶體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 14、一定條件下,VL的密閉容器中充入2molH2(氣)和2mol I2(氣),發生反應:H2(氣)+I2(氣)?2HI(氣),實驗過程中的速率與時間的變化關系如圖所示.下列說法正確的是( )
14、一定條件下,VL的密閉容器中充入2molH2(氣)和2mol I2(氣),發生反應:H2(氣)+I2(氣)?2HI(氣),實驗過程中的速率與時間的變化關系如圖所示.下列說法正確的是( )| A. | 陰影部分面積表示H2物質的量濃度的減少 | |
| B. | 反應達到限度時,H2、I2、HI的物質的量濃度比一定為1:1:2 | |
| C. | 當容器中密度保持不變時,說明反應一定達到平衡狀態 | |
| D. | 若0~10s內,HI的平均速率為0.01mol/(L•s),10s時H2余1.9mol,則容器體積V為2L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 路線:
路線:
 .
.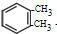 +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$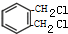 +2HCl
+2HCl
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
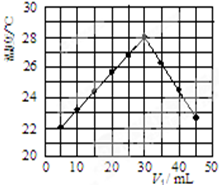 (一)實驗方法測定反應熱---------中和熱測定
(一)實驗方法測定反應熱---------中和熱測定| 實 驗 用 品 | 溶 液 溫 度 | 中和熱△H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1Cl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 煤的干餾是物理變化 | |
| B. | 石油裂解的目的主要是為了得到更多的汽油 | |
| C. | 石油分餾能得到不同沸點范圍的產物 | |
| D. | 石油裂化主得到的是乙烯、丙烯等 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
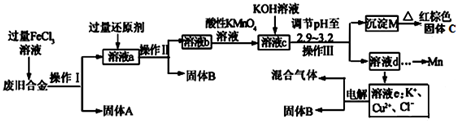
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com