
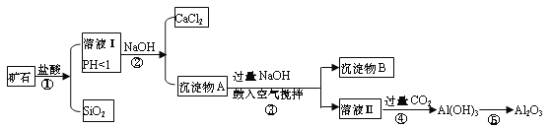
【題目】榴石礦石可以看作CaO、FeO、Fe2O3、Al2O3、SiO2組成。工業上對其進行綜合利用的流程如下:
(1)用方程式表示盛放氫氧化鈉溶液的試劑瓶不能用玻璃塞的原因________;
(2)溶液Ⅰ中除了Ca2+外,還可能含有的金屬陽離子有_______________;
(3)步驟③中NaOH參加反應的離子方程式是________________,鼓入空氣并充分攪拌的目的是_____________________。
(4)在工業生產中,步驟④通入過量CO2而不加入鹽酸的原因是___________;寫出步驟④通入過量CO2的離子方程式 _________________________________。
(5)試設計實驗證明榴石礦中含有FeO(試劑任選,說明實驗操作與現象)_________。
【答案】2 NaOH+SiO2 =Na2 SiO3 +H2OH+、Al3+、Fe3+ 、Fe2+Al (OH)3+OH-===AlO2-+2H2O使氫氧化亞鐵全部轉化為氫氧化鐵使用二氧化碳可以避免鹽酸過量導致生成的氫氧化鋁溶解,同時二氧化碳容易制取且價格便宜AlO2-+2H2O + CO2 =Al (OH)3 +HCO3-取少量礦石,加稀硫酸溶解后,向其中滴加酸性的高錳酸鉀溶液,若紫色退去,證明礦石中含有FeO (加鹽酸溶解或取溶液Ⅰ進行實驗不得分)
【解析】
榴石礦石可以看作CaO、FeO、Fe2O3、A12O3、SiO2組成,加入鹽酸溶解過濾得到濾液中含氯化鈣、氯化亞鐵、氯化鐵、氯化鋁、鹽酸,固體為SiO2,溶液中加入氫氧化鈉反應生成氫氧化鐵、氫氧化亞鐵、氫氧化鋁,過濾得到沉淀物A加熱過量氫氧化鈉通入空氣,氧化氫氧化亞鐵生成沉淀物氫氧化鐵和溶液Ⅱ為偏鋁酸鈉溶液,通入過量二氧化碳生成氫氧化鋁沉淀,加熱分解生成氧化鋁;
(1)二氧化硅是酸性氧化物和堿反應生成鹽和水;
(2)溶液Ⅰ除去鈣離子,含有陽離子H+、Fe2+、Fe3+、Al3+;
(3)步驟③中NaOH參加反應和氫氧化鋁反應生成偏鋁酸鈉溶液,鼓入空氣充分攪拌是為了氫氧化亞鐵氧化為氫氧化鐵;
(4)步驟④通入過量CO2而不加入鹽酸的原因是避免鹽酸過量使氫氧化鋁溶解,二氧化碳制備方法簡單價格便宜,過濾的二氧化碳和偏鋁酸鈉反應生成氫氧化鋁沉淀和碳酸氫鈉;
(5)取少量礦石加入稀硫酸溶解后加入高錳酸鉀溶液若褪色證明含有氧化亞鐵。
榴石礦石可以看作CaO、FeO、Fe2O3、A12O3、SiO2組成,加入鹽酸溶解過濾得到濾液中含氯化鈣、氯化亞鐵、氯化鐵、氯化鋁、鹽酸,固體為SiO2,溶液中加入氫氧化鈉反應生成氫氧化鐵、氫氧化亞鐵、氫氧化鋁,過濾得到沉淀物A加熱過量氫氧化鈉通入空氣,氧化氫氧化亞鐵生成沉淀物氫氧化鐵,和溶液Ⅱ為偏鋁酸鈉溶液,通入過量二氧化碳生成氫氧化鋁沉淀,加熱分解生成氧化鋁;
(1)玻璃中的二氧化硅和氫氧化鈉溶液反應,生成硅酸鈉和水,反應的化學方程式為:2NaOH+SiO2=Na2SiO3+H2O,
故答案為:2NaOH+SiO2=Na2SiO3+H2O;
(2)依據流程分析判斷,溶液Ⅰ除去鈣離子,含有陽離子Fe2+、Fe3+、Al3+,溶液ⅠpH<1,說明鹽酸過量,溶液中還含有H+,
故答案為:H+、Fe2+、Fe3+、Al3+;
(3)步驟③中NaOH參加反應和氫氧化鋁反應生成偏鋁酸鈉溶液,反應的離子方程式為:Al(OH)3+OH﹣═AlO2-+2H2O,鼓入空氣充分攪拌是為了氫氧化亞鐵氧化為氫氧化鐵,
故答案為:Al(OH)3+OH﹣═AlO2-+2H2O;使氫氧化亞鐵全部轉化為氫氧化鐵;
(4)步驟④通入過量CO2而不加入鹽酸的原因是避免鹽酸過量使氫氧化鋁溶解,二氧化碳制備方法簡單價格便宜,步驟④通入過量CO2的反應是二氧化碳和偏鋁酸鈉溶液反應生成氫氧化鋁沉淀和碳酸氫鈉,反應的離子方程式為:AlO2-+2H2O + CO2 =Al (OH)3 +HCO3-,
故答案為:使用二氧化碳可以避免鹽酸過量導致生成的氫氧化鋁溶解,同時二氧化碳容易制取且價格便宜;AlO2-+2H2O + CO2 =Al (OH)3 +HCO3-;
(5)取少量礦石,加稀硫酸溶解后,向其中滴加酸性的高錳酸鉀溶液,若紫色退去,證明礦石中含有FeO,
故答案為:取少量礦石,加稀硫酸溶解后,向其中滴加酸性的高錳酸鉀溶液,若紫色退去,證明礦石中含有FeO。


 一諾書業暑假作業快樂假期云南美術出版社系列答案
一諾書業暑假作業快樂假期云南美術出版社系列答案科目:高中化學 來源: 題型:
【題目】元素周期表中第三周期包括Na、Mg、Al、Si、P、S、Cl、Ar 8種元素。請回答下列問題:
(1)基態磷原子核外有________種運動狀態不同的電子。
(2)第三周期8種元素按單質熔點(℃)大小順序繪制的柱形圖(已知柱形“1”代表Ar)如下所示,則其中“2”原子的結構示意圖為________,“8”單質晶體的類型為________。


(3)氫化鎂
儲氫材料的晶胞結構如圖所示,已知該晶體的密度為ρ g·cm-3,則該晶體的化學式為________,晶胞的體積為________cm3(用ρ、NA表示,其中NA表示阿伏加德羅常數的值)。
(4)實驗證明:KCl、MgO、CaO三種晶體的結構與NaCl晶體的結構相似,已知NaCl、KCl、CaO晶體的晶格能數據如下表:
晶體 | NaCl | KCl | CaO |
晶格能/(kJ·mol-1) | 786 | 715 | 3 401 |
則KCl、MgO、CaO三種晶體的熔點從高到低的順序是________________。其中MgO晶體中一個Mg2+周圍和它最近且等距離的Mg2+有________個。
(5)Si、C和O的成鍵情況如下:
化學鍵 | C-O | C=O | Si-O | Si=O |
鍵能/(kJ·mol-1) | 360 | 803 | 464 | 640 |
C和O之間易形成含有雙鍵的CO2分子晶體,而Si和O之間則易形成含有單鍵的SiO2原子晶體,請結合數據分析其原因:__________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】隨原子序數遞增,八種短周期元素(用字母x等表示)原子半徑的相對大小、最高正價或最低負價的變化如下圖所示。

根據判斷出的元素回答問題:
上述元素可組成鹽R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的燒杯中滴加1mol·L-1NaOH溶液,沉淀物質的量隨NaOH溶液體積的變化示意圖如下:

(1)R溶液中,離子濃度由大到小的順序是___________________________________
(2)寫出m點反應的離子方程式:__________________________________________。
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反應后,溶液中產生沉淀的物質的量為________ mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】除去NaCl中含有的Ca2+、Mg2+、SO42-、HCO3-等離子,通常采用以下四種試劑:
①Na2CO3 ②BaCl2 ③NaOH ④HCl。加入試劑合理的操作順序是
A.①②③④B.③①②④C.③②①④D.④②①③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業合成氨的反應為N2(g)+3H2(g)![]() 2NH3(g)是一個放熱的可逆反應,反應條件是高溫、高壓,并且需要合適的催化劑。已知形成1 mol H—H鍵、1 mol N—H鍵、1 mol N≡N鍵放出的能量分別為436 kJ、391 kJ、946 kJ。則:
2NH3(g)是一個放熱的可逆反應,反應條件是高溫、高壓,并且需要合適的催化劑。已知形成1 mol H—H鍵、1 mol N—H鍵、1 mol N≡N鍵放出的能量分別為436 kJ、391 kJ、946 kJ。則:
(1)若1 mol氮氣完全反應生成氨氣可放出的能量為________ kJ。
(2)如果將1 mol氮氣和3 mol氫氣混合,使充分反應,反應放出的能量總小于上述數值,為什么___________?
(3)實驗室模擬工業合成氨時,在容積為2 L的密閉容器內,反應經過10分鐘后,生成10 mol 氨氣,則用氮氣表示的化學反應速率是________ mol·L-1·min-1。
(4)一定條件下,當合成氨的反應達到化學平衡時,下列說法正確的是________。
a.正反應速率和逆反應速率相等
b.正反應速率最大,逆反應速率為0
c.氮氣的轉化率達到最大值
d.氮氣和氫氣的濃度相等
e.N2、H2和NH3的體積分數相等
f.反應達到最大程度
(5)根據題目所給條件,判斷影響該反應速率的因素有________、________、__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Cu2O是一種鮮紅色粉末狀固體,幾乎不溶于水,在酸性溶液中歧化為二價銅和銅單質。可用于制造船底防污漆等。某校合作學習小組的同學設計實驗驗證其某些性質及其膠體的制法。回答下列問題:
(1)甲組同學檢驗H2還原CuO所得的紅色粉末中是否有Cu2O。取反應產物少許加入試管中,加入足量的試劑X并攪拌,若發現溶液變藍且仍有剩余固體,則試劑X可選用_________(填序號)。
a.FeCl3溶液 b.硝酸 c.稀硫酸 d. H2O2酸性溶液
(2)乙組同學在兩支試管中分別加入少量Cu2O,一支中加入稀硝酸,固體溶解同時產生NO氣體,Cu2O表現_______________性;另一支加入硫酸酸化的KMnO4溶液,溶液紫色褪去得藍色溶液,反應的離子方程式為______________。
(3)丙組同學取少量Cu2O與黑色的Cu2S混合加強熱,產生大量的氣體同時得到紅色固體粉末,該反應的化學方程式為____________________。
(4)丁組同學向0.1mol·L-1 的(CH3COO)2Cu溶液中加入0.02mol·L-1的N2H4的水溶液,控制pH=7~8,得到紅色透明液體,能說明該分散系屬于膠體的簡單方法是____________。已知制備過程中有N2放出,制備反應的化學方程式為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某鐵的氧化物(FexO)1.52 g溶于足量鹽酸中,向所得溶液中通入標準狀況下112 mL Cl2,恰好將Fe2+完全氧化。下列說法正確的是( )
A. FexO溶于足量鹽酸后只生成了FeCl3和H2O
B. 標準狀況下112 mL Cl2的物質的量是5 mol
C. x=0.8
D. 通入Cl2后,發生反應的離子方程式:Fe2++Cl2![]() Fe3++2Cl﹣
Fe3++2Cl﹣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2015年10月5日,中國著名藥學家屠呦呦獲得諾貝爾獎生理學或醫學獎,獲獎理由是“因為發現青蒿素一一種用于治療瘧疾的藥物,挽救了全球特別是發展中國家的數百萬人的生命”。青蒿素是從植物黃花蒿莖葉中提取的,其結構簡式如下圖,下列說法不正確的是
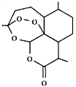
A. 它的分子式為C15H22O5
B. 該分子中有6個手性碳原子
C. 因其具有過氧基團,它不穩定,易受濕、熱和還原性物質的影響而變質
D. 它在常見有機溶劑中的溶解度大于在水中的溶解度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C為中學常見單質,其中一種為金屬;通常情況下A為固體、B為黃綠色氣體、C為無色氣體。D、E、F、G、H、X均為化合物,其中X常溫下是無色氣體,其水溶液是一種無氧強酸溶液,E為黑色固體,H在常溫下為液體。它們之間的轉化關系如圖所示(其中某些反應條件和部分反應產物已略去)。
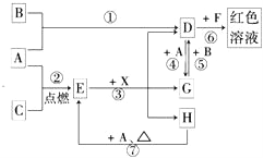
(1)寫出下列物質的化學式:D___________,X_______________。
(2)在反應①~⑦中,不屬于氧化還原反應的是_____________(填編號)。
(3)反應⑥的離子方程式為:______________________________________。
(4)往G溶液中加入NaOH溶液觀察到的現象是________________________。
(5)反應⑦的化學方程式為____________________________________;該反應中每消耗0.3mol的A,可轉移電子________mol。
(6)除去D溶液中混有的少量G的化學方程式:_________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com