
| A. | 30gSiO2晶體中含有NA個硅氧鍵 | |
| B. | 常溫常壓下,11.2LCl2含有的分子數目少于0.5NA | |
| C. | 25℃時,pH=12的NaOH溶液含有的OH-數目為0.01NA | |
| D. | 50mL18.4mol/L濃硫酸與足量銅微熱,生成SO2分子的數目為0.46NA |
分析 A.1molSiO2晶體含有4mol的硅氧鍵;
B.常溫常壓Vm大于22.4L/mol;
C.溶液體積未知;
D.銅只與濃硫酸反應,與稀硫酸不反應;
解答 解:A.30gSiO2晶體物質的量為$\frac{30g}{60g/mol}$=0.5mol,含有硅氧鍵數為0.5mol×4×NA=2NA,故A錯誤;
B.常溫常壓Vm大于22.4L/mol,所以11.2LCl2含有氯氣分子的物質的量小于0.5mol,含有的分子數目少于0.5NA,故B正確;
C.溶液體積未知,無法計算氫氧根子數目,故C錯誤;
D.隨著反應進行,硫酸濃度變稀,與銅將不再反應,生成二氧化硫小于0.46mol,故D錯誤;
故選:B.
點評 本題考查阿伏伽德羅常數的計算與判斷,題目難度中等,涉及知識點較多、綜合性較強,充分考查學生的分析、理解能力及靈活應用基礎知識的能力,注意熟練掌握物質的量與阿伏伽德羅常數、摩爾質量等物理量之間的關系.


 世紀百通期末金卷系列答案
世紀百通期末金卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | -48.5kJ/mol | B. | +48.5kJ/mol | C. | -45.5kJ/mol | D. | +45.5kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 78g過氧化鈉中含2NA個O2- | |
| B. | 0.1molOH-含NA個電子 | |
| C. | 1.8g重水(D2O)中含NA個中子 | |
| D. | 標準狀況下11.2L臭氧中含NA個氧原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在100 g質量分數為30%的甲醛水溶液中,含有氫原子數為2NA | |
| B. | 7.8 g Na2S和Na2O2固體混合物中,含有的陰離子數為0.1NA | |
| C. | 1mol乙醇含有共價鍵的總數7NA | |
| D. | 反應2SO2(g)+O2(g)?2 SO3 (g),單位時間內消耗NA個O2分子的同時生成2NA個SO3分子,此時反應達到平衡狀態 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3C(s)+CaO(s)═CaC2(s)+CO(g)在常溫下不能自發進行,說明該反應的△H>0 | |
| B. | 0.1mol/L氨水加水稀釋后,溶液中$\frac{c(O{H}^{-})}{c(N{{H}_{3}•{H}_{2}O}_{\;})}$的值減小 | |
| C. | 常溫常壓下,22.4L Cl2中含有的分子數為6.02×1023個 | |
| D. | 合成氨時,其他條件不變,升高溫度,氫氣的反應速率和平衡轉化率均增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 9 g超重水(3H216O)含中子數為6NA | |
| B. | 標準狀況下,22.4 L CCl4含有的分子數目為NA | |
| C. | 常溫常壓下,16g甲烷中共價鍵數目為4NA | |
| D. | 1 L 0.1 mol•L-1的NaHCO3溶液中HCO3-和CO32-離子數之和為0.1 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 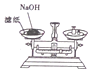 稱取一定量的NaOH | |
| B. | 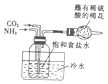 制取NaHCO3 | |
| C. | 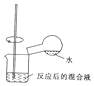 檢驗濃硫酸與銅反應后的產物中是否含有銅離子 | |
| D. | 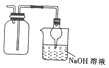 收集NO2丙防止其污染環境 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧化鋇溶液和硫酸鈉溶液混合:Ba2++SO42-=BaSO4↓ | |
| B. | 將亞硫酸氫鈉加入鹽酸溶液中:HSO3-+H+=SO2↑+H2O | |
| C. | 氫硫酸與亞硫酸混合:H2SO3+2H2S=3S↓+3H2O | |
| D. | H2S氣體通入CuSO4溶液中:Cu2++S2-=CuS↓ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com