
分析 (1)根據題意可知,當Fe2+以Fe(OH)2的形式完全沉淀時,Cu2+已經沉淀完畢,所以除去亞鐵離子時不能除去銅離子,則應該調節溶液pH且將亞鐵離子轉化為鐵離子;
(2)亞鐵離子具有還原性、次氯酸根離子具有氧化性,二者發生氧化還原反應生成鐵離子和氯離子,鐵離子和次氯酸根離子能發生雙水解反應;
(3)在調整pH的同時應不帶入新的雜質離子,加入的固體要和氫離子反應;
(4)當c(Cu2+)為1 mol/L時,代入關系式lg c(Cu2+)=8.6-2pH,可解得pH=4.3,再結合鐵離子和pH關系判斷鐵離子是否完全沉淀.
解答 解:(1)根據題意可知,當Fe2+以Fe(OH)2的形式完全沉淀時,Cu2+已經沉淀完畢,因此欲除去Fe2+,應先將Fe2+氧化成Fe3+,再調節溶液的pH在3~4之間,所以其采用的方法是:先將Fe2+氧化成Fe3+,再調節溶液的pH在3~4之間,
故答案為:先將Fe2+氧化成Fe3+,再調節溶液的pH在3~4之間;
(2)根據題意當氧化劑選用NaClO時,NaClO先將Fe2+氧化,次氯酸根離子和Fe3+發生雙水解反應,其反應的離子方程式可表示為:2Fe2++ClO-+2H+=2Fe3++Cl-+H2O,Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO,很顯然,隨著反應的進行,氫離子濃度降低,則溶液的pH增大,Fe3+同樣開始沉淀,
故答案為:2Fe2++ClO-+2H+=2Fe3++Cl-+H2O,Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO;增大;
(3)在調整pH的同時應不帶入新的雜質離子,因此可選用難溶于水的氧化銅或氫氧化銅等固體,
故答案為:CuO或Cu(OH)2;
(4)當c(Cu2+)為1 mol/L時,代入關系式lg c(Cu2+)=8.6-2pH,可解得pH=4.3,此時溶液中的Fe3+能沉淀完全,
故答案為:4.3;能.
點評 本題考查物質分離、提純的綜合應用,明確物質性質是解本題關鍵,側重考查學生獲取信息利用信息解答問題能力,注意除雜時不能引進新的雜質,注意亞鐵離子除去方法,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 0.1mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) | |
| B. | pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液:c(CH3COONa)>c(Na2CO3)>c(C6H5ONa )>c(NaOH ) | |
| C. | NH4HSO4溶液中滴加NaOH溶液至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) | |
| D. | 在飽和氯水中加入NaOH使pH=7,所得溶液中存在下列關系:c(Na+)>c(ClO-)>c(Cl-)>c(HClO) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
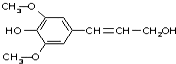 膳食纖維具有突出的保鍵功能,是人體的“第七營養素”.木質素是一種非糖類膳食纖維,其單體之一是芥子醇,結構簡式如圖所示.下列有關芥子醇的說法正確的是( )
膳食纖維具有突出的保鍵功能,是人體的“第七營養素”.木質素是一種非糖類膳食纖維,其單體之一是芥子醇,結構簡式如圖所示.下列有關芥子醇的說法正確的是( )| A. | 芥子醇能發生的反應類型有氧化、取代、水解、加聚 | |
| B. | 芥子醇的分子式是C11H14O4,屬于芳香烴 | |
| C. | 芥子醇分子中所有碳原子可能在同一平面 | |
| D. | 芥子醇能與3mol溴水反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
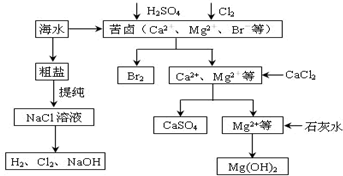

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 元素 | 部分結構知識 | 部分性質 |
| X | X原子核外電子占有9個原子軌道 | X的一種氧化物是形成酸雨的主要物質 |
| Y | Y原子的次外層電子數等于最外層電子數的一半 | Y能形成多種氣態氫化物 |
| Z | Z原子的最外層電子數多于4 | Z元素的最高正化合價與最低負化合價代數和等于6 |
| W | W原子的最外層電子數等于2n-3(n為原子核外電子層數) | 化學反應中W原子易失去最外層電子形成Wn+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
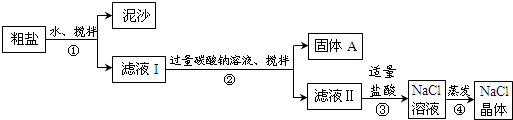
| 猜想 | 驗證的方法 | 現象 | 結論 |
| 猜想Ⅰ:固體A中含CaCO3、MgCO3 | 取少量固體A于試管中,滴加稀鹽酸,并用涂有澄清石灰水的小燒杯罩于試管口 | ①有氣泡冒出且澄清石灰水變渾濁 | 猜想Ⅰ成立 |
| 猜想Ⅱ:固體A中含BaCO3 | 取少量固體A于試管中,先滴入②稀鹽酸或稀硝酸,再滴入Na2SO4溶液 | 有氣泡放出,無白色沉淀 | ③猜想II不成立 |
| 猜想Ⅲ:最后制得的NaCl晶體中還含有Na2SO4 | 取少量NaCl晶體溶于試管中的蒸餾水, ④加入硝酸酸化的硝酸鋇溶液 | ⑤產生不溶于稀硝酸的白色沉淀 | 猜想Ⅲ成立 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在1 mol•L-1的KClO3溶液中,K+的個數為NA | |
| B. | 在標準狀況下,22.4 L CH3CH2OH的分子數為NA | |
| C. | 32 g氧氣和臭氧的混和氣體中含有的氧原子數為2NA | |
| D. | 22.4 L HCl氣體中含有的分子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HCl和NaOH反應的中和熱△H=-57.3 kJ/mol,則H2SO4和Ca(OH)2反應的中和熱△H=2×(-57.3)kJ/mol | |
| B. | CO(g)的燃燒熱是283.0 kJ/mol,則2CO2(g)=2CO(g)+O2(g)反應的△H=+566.0 kJ/mol | |
| C. | 需要加熱才能發生的反應一定是吸熱反應 | |
| D. | Ba(OH)2•8H2O與NH4Cl反應的焓變小于0,所以在常溫下能自發進行 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯化氫的電子式為 H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$]- | |
| B. | 乙炔的結構簡式(刪:可以)寫成 CHCH | |
| C. | 鎂的原子結構示意圖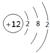 | |
| D. | 碳酸氫鈉溶于水電離方程式:NaHCO3═Na++H++CO32- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com