
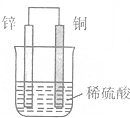
| A. | 鋅片上有H2逸出 | B. | 溶液中c(H+)逐漸減小 | ||
| C. | 正極反應式:2H++2e-═H2↑ | D. | 負極反應式:Zn-2e-═Zn2+ |
分析 該原電池中,Zn易失電子作負極、Cu作正極,負極反應式為Zn-2e-═Zn2+,正極反應式為2H++2e-═H2↑,據此分析解答.
解答 解:該原電池中,Zn易失電子作負極、Cu作正極,
A.鋅電極上Zn失電子生成鋅離子進入溶液,正極上氫離子得電子生成氫氣,所以銅片上有氫氣逸出,故A錯誤;
B.正極上氫離子放電生成氫氣,導致溶液中c(H+)逐漸減小,故B正確;
C.正極上氫離子放電生成氫氣,電極反應式為2H++2e-═H2↑,故C正確;
D.負極上鋅失電子發生氧化反應,電極反應式為Zn-2e-═Zn2+,故D正確;
故選A.
點評 本題考查原電池原理,為高頻考點,明確正負極判斷方法及各個電極上發生的反應是解本題關鍵,會正確書寫電極反應式,題目難度不大.


科目:高中化學 來源: 題型:多選題
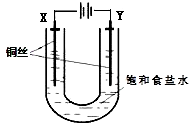 已知:Ksp(CuCl,白色)=1.2×10-6,Ksp(CuOH,橙黃色)=1.2×10-14.如圖,用銅電極電解飽和食鹽水時,陽極發生的電極反應為Cu-e-+Cl-═CuCl.下列說法不正確的是( )
已知:Ksp(CuCl,白色)=1.2×10-6,Ksp(CuOH,橙黃色)=1.2×10-14.如圖,用銅電極電解飽和食鹽水時,陽極發生的電極反應為Cu-e-+Cl-═CuCl.下列說法不正確的是( )| A. | Y極發生的電極反應2H2O+2e-═2OH-+H2↑ | |
| B. | 實驗開始時,X極附近出現白色渾濁 | |
| C. | 一段時間后,U形管底部形成橙黃色沉淀 | |
| D. | 電解時,Cl-移向Y極 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 的下列敘述中,正確的是( )
的下列敘述中,正確的是( )| A. | 它的系統名稱是2,4-二甲基-4-戊烯 | |
| B. | 它的分子中最多有5個碳原子在同一平面上 | |
| C. | 它與甲基環己烷互為同分異構體 | |
| D. | 有機物的一氯取代產物共有4種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 活化分子間所發生的碰撞都為有效碰撞 | |
| B. | 合成氨工業中用鐵觸媒做催化劑能用勒夏特列原理解釋 | |
| C. | 升高溫度能使化學反應速率增大的主要原因是增加了單位體積內活化分子的百分數 | |
| D. | 將鋼閘門與電源的正極相連,是采用了外加電流的陰極保護法 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
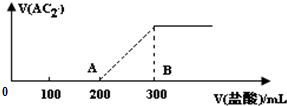 A、B、C、D、E為原子序數依次增大的五種短周期元素,A、B、C位于同一周期,C、E位于同一主族,A元素在自然界中形成的化合物種類最多,C元素的氫化物是最常用的溶劑,D元素在同周期元素中離子半徑最小.請回答:
A、B、C、D、E為原子序數依次增大的五種短周期元素,A、B、C位于同一周期,C、E位于同一主族,A元素在自然界中形成的化合物種類最多,C元素的氫化物是最常用的溶劑,D元素在同周期元素中離子半徑最小.請回答: ;D元素的最高價氧化物的水化物的電離方程式Al(OH)3?Al3++3OH-.
;D元素的最高價氧化物的水化物的電離方程式Al(OH)3?Al3++3OH-.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 三個燒杯中一定均會發生的離子反應有:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 三個燒杯中鈉均在液面上劇烈反應 | |
| C. | Z燒杯中一定會有沉淀生成,但沉淀不是單質銅 | |
| D. | 三個燒杯中生成氫氣的物質的量相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
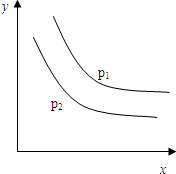
| A. | 上述反應是放熱反應 | B. | 上述反應是吸熱反應 | ||
| C. | a+b>c | D. | a+b<c |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 潤洗酸式滴定管時應從滴定管上口加入3~5mL所要盛裝的酸溶液,傾斜著轉動滴定管,使液體潤濕其內壁,再從上口倒出,重復2~3次 | |
| B. | 用惰性電極電解MgCl2溶液的離子方程式為:2Cl-+2H2O$\frac{\underline{\;電解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 為驗證鹽橋的作用,在兩個燒杯中分別盛適量硫酸亞鐵銨溶液和稀酸性高錳酸鉀溶液,分別插入石墨棒用導線與電流計相連,然后用裝有K2SO4飽和溶液的瓊脂的U型管兩端插入兩個燒杯中,電流計偏轉,一段時間后高錳酸鉀溶液褪色 | |
| D. | 嫦娥三號月球車玉兔號在進入第二個月夜休眠前,出現了機構控制異常情況,其病因或為月塵,即月球上直徑小于10微米的浮塵,月塵分散在空氣中形成的分散系屬于膠體 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com