
分析 (1)根據m=nM計算質量之比,根據N=nNA計算分子數目之比,結合分子式計算原子數目、H原子數目之比;
(2)根據m=nM計算二氧化碳的質量,根據N=nNA計算二氧化碳分子數目,根據V=nVm計算二氧化碳的體積,氧原子物質的量為二氧化碳的2倍;
(3)根據m=nM計算質量之比,根據N=nNA計算分子數目之比,結合分子式計算原子數目之比,根據V=nVm計算體積之比.
解答 解:(1)根據m=nM可知,等物質的量的CH4和NH3的質量比為16g/mol:17g/mol=16:17,根據N=nNA可知,二者分子個數比為1:1,由分子式可知,原子個數比為1×5:1×4=5:4,氫原子個數比為1×4:1×3=4:3,
故答案為:16:17;1:1;5:4;4:3;
(2)2mol CO2的質量為2mol×44g/mol=88g,含分子數約為2mol×6.02×1023mol-1=1.204×1024,在標準狀況下所占有的體積約為2mol×22.4L/mol=44.8L,含氧原子的物質的量為2mol×2=4mol,
故答案為:88;1.204×1024;44.8;4;
(3)0.3mol的氧氣和0.2mol的臭氧O3,它們的質量之比是0.3mol×32g/mol:0.2mol×48g/mol=1:1,含有分子數之比是0.3mol:0.2mol=3:2,原子數之比是3×2:2×3=1:1,它們的體積比(同溫、同壓)是0.3mol:0.2mol=3:2,
故答案為:1:1;3:2;1:1;3:2.
點評 本題考查物質的量有關計算,比較基礎,注意對公式的理解與靈活應用.


科目:高中化學 來源: 題型:解答題
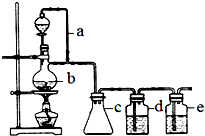 某研究性學習小組為合成1-丁醇,查閱資料得知一條合成路線:
某研究性學習小組為合成1-丁醇,查閱資料得知一條合成路線:查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
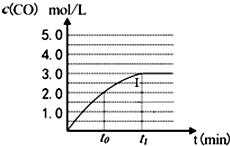 工業上一般在密閉容器中采用下列反應合成甲醇:
工業上一般在密閉容器中采用下列反應合成甲醇:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 漂白粉溶液中通入過量的CO2:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO | |
| B. | 氯氣與水的反應:Cl2+H2O═2H++Cl-+ClO- | |
| C. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| D. | 鈉和冷水反應:Na+2H2O═Na++2OH?+H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鹵代反應 | B. | 加聚反應 | C. | 酯化反應 | D. | 消去反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
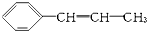 ,它可能具有的性質是( )
,它可能具有的性質是( )| A. | 易溶于水,也易溶于有機溶劑 | |
| B. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色 | |
| C. | 能發生聚合反應,其產物可表示為 | |
| D. | 能使溴水褪色,但不能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
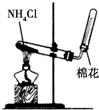 |  | 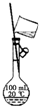 | 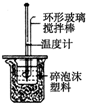 |
| A.實驗室制取氨氣 | B.測定反應速率裝置 | C.配制100 mL 0.1 mol/L鹽酸 | D.測定中和反應的反應熱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 硫完全燃燒生成二氧化硫時,放出的熱量為硫的標準燃燒熱 | |
| B. | 在101kPa時,1mol碳燃燒所放出的熱量為碳的標準燃燒熱 | |
| C. | 在101kPa時,由2CO(g)+O2(g)═2CO2(g)△H=-566 kJ•mol-1,可知CO的標準燃燒熱為283 kJ•mol-1 | |
| D. | 乙炔的標準燃燒熱為1299.6 kJ•mol-1,則2CH2(g)+5O2(g)═4CO2(g)+2H2O(g)反應的△H=-2 599.2 kJ•mol-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com