
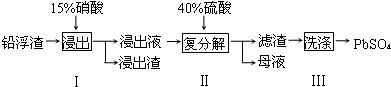
| 化學式 | CaSO4 | Ag2SO4 | PbSO4 |
| Ksp | 4.9×10-5 | 1.2×10-5 | 1.6×10-8 |
分析 鉛浮渣的主要成分是PbO、Pb還有少量的Ag、CaO,加入硝酸可以發生反應生成的主要是硝酸鉛溶液,向該浸出液中加入硫酸,可以發生復分解反應生成硫酸鉛沉淀和硝酸,硝酸可以循環使用,用來溶解PbO、Pb,過濾得到的沉淀是硫酸鉛,
(1)用75%的硝酸來配制15%的硝酸溶液,用量筒量取一定量的濃硝酸和水,在燒杯中配制,用玻璃棒攪拌,據此答題;
(2)鉛與硝酸反應生成一氧化氮和硝酸鉛,當鉛過量時銀不能溶解,據此答題;
(3)硝酸鉛與硫酸反應生成硫酸鉛和硝酸,硝酸可用于循環利用,若母液中殘留的 SO42-過多,在步驟I中就會有硫酸鉛沉淀出現,會隨浸出渣排出;
(4)根據流程可知,粗PbSO4 產品含有的雜質是硫酸鈣,可以用硝酸鉛溶液洗滌除去;
(5)鉛蓄電池放電時正極是氧化鉛得電子生成硫酸鉛,電解飽和食鹽水制取Cl2,當制得4.48LCl2時要轉移電子的物質的量為$\frac{4.48}{22.4}×2$mol=0.4mol,根據電子守恒可知,此時鉛蓄電池中也轉移0.4mol電子,根據鉛蓄電池的總反應可計算出消耗硫酸的物質的量,進而確定電解后電池中硫酸溶液的濃度.
解答 解:(1)用75%的硝酸來配制15%的硝酸溶液,用量筒量取一定量的濃硝酸和水,在燒杯中配制,用玻璃棒攪拌,所以用不到的儀器是容量瓶、錐形瓶,故選CD;
(2)鉛與硝酸反應生成一氧化氮和硝酸鉛,反應的方程式為3Pb+8HNO3=3Pb(NO3)2+2NO↑+4H2O,當鉛過量時銀不能溶解,所以為防止Ag被溶解進入溶液,步驟I操作時應注意控制硝酸的用量并使Pb稍有剩余,
故答案為:3Pb+8HNO3=3Pb(NO3)2+2NO↑+4H2O;控制硝酸的用量并使Pb稍有剩余;
(3)硝酸鉛與硫酸反應生成硫酸鉛和硝酸,硝酸可用于循環利用,若母液中殘留的 SO42-過多,在步驟I中就會有硫酸鉛沉淀出現,會隨浸出渣排出,
故答案為:HNO3;浸出時部分Pb2+生成PbSO4隨浸出渣排出,降低PbSO4的產率;
(4)根據流程可知,粗PbSO4 產品含有的雜質是CaSO4,可以用Pb(NO3)2溶液洗滌除去,
故答案為:CaSO4;Pb(NO3)2;
(5)鉛蓄電池放電時正極是氧化鉛得電子生成硫酸鉛,電極反應式為PbO2+2e-+4H++SO42-=PbSO4+2H2O,電解飽和食鹽水制取Cl2,當制得4.48LCl2時要轉移電子的物質的量為$\frac{4.48}{22.4}×2$mol=0.4mol,根據電子守恒可知,此時鉛蓄電池中也轉移0.4mol電子,根據鉛蓄電池的總反應可知H2SO4~1e-,所以消耗硫酸的物質的量為0.4mol,則電解后電池中硫酸溶液的濃度為$\frac{4.50mol•{L}^{-1}×0.80L-0.4mol}{0.80L}$=4mol/L,
故答案為:PbO2+2e-+4H++SO42-=PbSO4+2H2O;4.
點評 本題考查了生產硫酸鉛的工藝流程、硝酸的性質等,還涉及基本的實驗操作、原電池、化學計算等,考查學生分析問題和解決問題的能力,題目難度中等.


 海淀課時新作業金榜卷系列答案
海淀課時新作業金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 輕松課堂標準練系列答案
輕松課堂標準練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 二氧化硅是酸性氧化物,它可以跟強堿反應,但是不能與任何酸反應 | |
| B. | 根據SiO2+CaCO3$\frac{\underline{\;高溫\;}}{\;}$CaSiO3+CO2↑的反應,可推知硅酸酸性比碳酸強 | |
| C. | 二氧化碳氣體通入硅酸鈉溶液中可以制得硅酸 | |
| D. | 二氧化硅對應的水化物只有H2SiO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在鐵質船體上鑲嵌鋅塊,可以減緩船體被海水腐蝕的速率,稱為犧牲陰極的陽極保護法 | |
| B. | 電解飽和食鹽水是將電能轉變成化學能,在陰極附近生成氫氧化鈉和氫氣 | |
| C. | 銅鋅原電池反應中,銅片作正極,產生氣泡發生還原反應,電子從銅片流向鋅片 | |
| D. | 外加電流的陰極保護法是將被保護的金屬與外加電源的正極相連 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 該硫酸的物質的量濃度為9.2mol•L-1 | |
| B. | 用該硫酸配制稀硫酸時必須用到托盤天平 | |
| C. | 配制200mL 4.6mol/L的稀硫酸需量取該硫酸50mL | |
| D. | 該硫酸與等質量的水混合所得溶液的物質的量濃度大于9.2mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
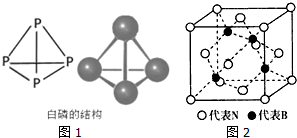 利用周期表中同族元素的相似性,可預測元素的性質.
利用周期表中同族元素的相似性,可預測元素的性質.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 18O原子核內的中子數為8 | B. | 16O2和18O2的化學性質幾乎相同 | ||
| C. | H216O與H218O質子數不同 | D. | H2和D2屬于同位素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2(HCl):通過水洗滌 | B. | NO(NH3):通過水洗滌 | ||
| C. | NH4Cl(NaCl):加熱混合物 | D. | NH4Cl溶液(I2):用CCl4萃取 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 新制的氯水在光照下顏色變淺 | |
| B. | 氫氧化鐵膠體加熱生成紅褐色沉淀 | |
| C. | 在合成氨的反應中,降溫或加壓有利于氨的合成 | |
| D. | Fe(SCN)3溶液中加入6mol/L NaOH溶液后顏色變淺 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com