
 g]
g]分析 方案一:(1)樣品稱量可以得到樣品質量為m1g,加入稀鹽酸溶解后,過濾得到溶液為氯化鈉溶液,蒸發濃縮結、冷卻結晶、洗滌、干燥得到氯化鈉,稱量得到固體氯化鈉的質量為m2g;
(2)溶解、蒸發結晶需要用到玻璃棒;
(3)操作③是從溶液中獲得晶體;
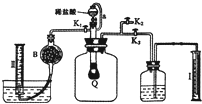
(4)反應產生的CO2、O2使氣球變大,將廣口瓶中氣體排出,水進入量筒Ⅰ中,所以量筒Ⅰ中水的體積即為產生的CO2、O2的體積;為使分液漏斗內液體順利流下,應是分液漏斗內外壓強相等;
(5)用堿石灰吸收二氧化碳,量筒Ⅱ中排出液態的體積為氧氣體積,氣流速度太快,不利于二氧化碳吸收;
(6)根據生成氧氣的體積計算過碳酸鈉反應生成二氧化碳的體積,結合二氧化碳的總體積可以計算碳酸鈉反應生成二氧化碳的體積,根據二氧化碳的可以起到過碳酸鈉與碳酸鈉的物質的量之比,進而計算過碳酸鈉的質量分數.
解答 解:樣品稱量可以得到樣品質量為m1g,加入稀鹽酸溶解后,過濾得到溶液為氯化鈉溶液,蒸發濃縮結、冷卻結晶、洗滌、干燥得到氯化鈉,稱量得到固體氯化鈉的質量為m2g.
(1)操作①為稱量固體質量,操作③為結晶得到氯化鈉固體,
故答案為:稱量;蒸發結晶;
(2)固體溶解需要玻璃棒攪拌加速溶解,溶液中得到溶質固體需要在蒸發皿中加熱蒸發結晶,過程中需要玻璃棒攪拌,受熱均勻,上述操作中,使用到玻璃棒的有②③,
故答案為:②③;
(3)溶液中得到溶質固體的方法是加熱蒸發結晶析出,具體操作為:得到的溶液在蒸發皿中加熱蒸發,用玻璃棒不斷攪拌到大量晶體析出,停止加熱靠余熱蒸發剩余的水分得到氯化鈉固體,
故答案為:得到的溶液在蒸發皿中加熱蒸發,用玻璃棒不斷攪拌到大量晶體析出,停止加熱靠余熱蒸發剩余的水分得到氯化鈉固體;
(4)反應產生的CO2、O2使氣球變大,將廣口瓶中氣體排出,水進入量筒Ⅰ中,所以量筒Ⅰ中水的體積即為產生的CO2、O2的體積,所以滴稀H2SO4前必須關閉K1、K2打開K3,為使分液漏斗內液體順利流下,應是分液漏斗內外壓強相等,所以導管a的作用是平衡分液漏斗上下的壓強使順利流下,
故答案為:K1、K2;K3; 平衡分液漏斗上下的壓強使順利流下;
(5)用堿石灰吸收二氧化碳,量筒Ⅱ中排出液態的體積為氧氣體積,緩緩打開K1,讓生成的二氧化碳能充分被b中堿石灰吸收,使量筒內收集到純凈的氧氣,
故答案為:堿石灰;讓生成的二氧化碳能充分被b中堿石灰吸收,使量筒內收集到純凈的氧氣;
(6)量筒I中有xmL水,則CO2、O2的總體積為xmL,量筒Ⅱ中收集到了ymL氣體,則O2總體積為y mL,則反應2Na2CO4+4HCl═4NaCl+2CO2+O2+2H2O,生成的二氧化碳為2y mL,碳酸鈉反應生成二氧化碳為(x-y-2y)=(x-3y) mL,生成二氧化碳物質的量之比為2y:(x-3y),則Na2CO4與碳酸鈉的物質的量之比為2y:(x-3y),故樣品中過碳酸鈉的質量分數是$\frac{2y×122}{2y×122+(x-3y)×106}$=$\frac{122y}{53x-37y}$,
故答案為:$\frac{122y}{53x-37y}$.
點評 本題考查了物質含量的實驗測定方法,關鍵是理解測定原理,定量實驗中盡可能減小誤差,(6)中計算為易錯點,注意測量氣體的體積不一定是標況下,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分子式為C3H6Cl2的同分異構體有四種 | |
| B. | 分子式為C8H10的芳香烴有3個,分別為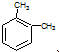 、 、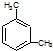 和 和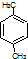 | |
| C. | 分子式為C4H8的烯烴同分異構體有2個,分別為CH2=CHCH2CH3、CH3CH=CHCH3 | |
| D. | 二氯甲烷有兩種同分異構體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ca2+:1s22s22p63s23p6 | B. | O:1s22s22p6 | ||
| C. | P:1s22s22p63s23p3 | D. | Br:1s22s22p63s23p63d104s24p5 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
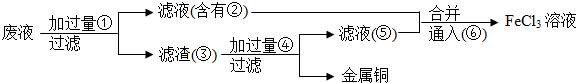
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
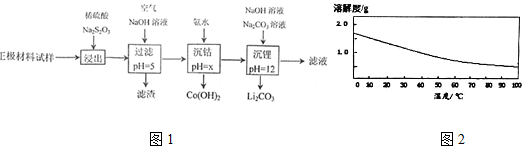
| 氫氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)3 |
| 開始沉淀的pH | 3.1 | 7.1 | 2.2 |
| 完全沉淀的pH | 4.7 | 9.7 | 3.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 人體缺碘,可通過食用加碘鹽補碘 | |
| B. | 缺鐵性貧血,可通過食用鐵強化醬油預防 | |
| C. | 鋅攝入量過多,也會引起缺鐵性貧血 | |
| D. | 為了防止齲齒,人人都適合使用含氟牙膏 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 熔點/℃ | 密度/g.cm-3 | 硬度 | 導電性 | |
| 某合金 | 2500 | 3.00 | 7.4 | 2.3 |
| 鐵 | 1535 | 7.86 | 4.5 | 17 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
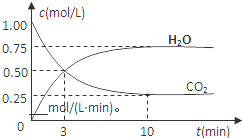
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com