
下列敘述正確的是
A. 向2mL2%的CuSO4溶液中加入幾滴1%的NaOH溶液,振蕩后再加入0.5mL有機物X,加熱后未出現磚紅色沉淀,說明X結構中不含有醛基
B. 室溫下向苯和少量苯酚的混合溶液中加入適量濃溴水,振蕩、靜置后過濾,可除去苯中少量苯酚
C. 向溴水中滴入植物油,振蕩后,油層顯無色,說明溴不溶于油脂
D. 使用含NaF的牙膏,可以使牙齒上的Ca5(PO4)3OH轉化為Ca5(PO4)3F,防止蛀牙,說明Ksp[Ca5(PO4)3F]< Ksp[Ca5(PO4)3OH]
科目:高中化學 來源:2016-2017學年黑龍江省高一下學期開學考試化學試卷(解析版) 題型:選擇題
已知硫酸鉛難溶于水,也難溶于硝酸,卻可溶于醋酸銨溶液中,形成無色的溶液,其化學方程式是:PbSO4+2NH4Ac Pb(Ac)2+(NH4)2SO4。當Pb(Ac)2(醋酸鉛)溶液中通入H2S時,有黑色沉淀PbS和弱電解質HAc生成。表示這個反應的有關離子方程式正確的是( )
Pb(Ac)2+(NH4)2SO4。當Pb(Ac)2(醋酸鉛)溶液中通入H2S時,有黑色沉淀PbS和弱電解質HAc生成。表示這個反應的有關離子方程式正確的是( )
A. Pb(Ac)2+H2S PbS↓+2HAc
PbS↓+2HAc
B. Pb2++H2S PbS↓+2H+
PbS↓+2H+
C. Pb2++2Ac-+H2S PbS↓+2HAc
PbS↓+2HAc
D. Pb2++2Ac-+2H++S2— PbS↓+2HAc
PbS↓+2HAc
查看答案和解析>>
科目:高中化學 來源:遼寧省大連市2017屆高三3月雙基測試化學試卷 題型:簡答題
CO和H2均是重要的化工原料,CO2的固定和利用對環境保護及能源開發具有重要的意義。
(1)利用水煤氣(CO+H2)作為合成氣,在同一容器中,選擇雙催化劑,經過如下三步反應,最終合成二甲醚(CH3OCH3)。
甲醇合成反應:CO(g)+2H2(g) CH3OH(g) △H1=-90.8kJ·mol-1
CH3OH(g) △H1=-90.8kJ·mol-1
水煤氣變換反應:CO(g)+H2O(g) CO2(g)+H2(g) △H2=-41.3kJ·mol-1
CO2(g)+H2(g) △H2=-41.3kJ·mol-1
甲醇脫水反應:2CH3OH(g) CH3OCH3(g)+H2O(g) △H3=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H3=-23.5kJ·mol-1
寫出由CO和H2合成二甲醚氣體和水蒸氣的熱化學方程式____________。
(2)在2L恒容密閉容器中,投入CO(g)和H2(g)各5mol,發生如下反應:
3CO(g)+3H2(g) CH3OCH3(g)+CO2(g) △H<0,CO的轉化率α與溫度、壓強的關系如圖所示:
CH3OCH3(g)+CO2(g) △H<0,CO的轉化率α與溫度、壓強的關系如圖所示:
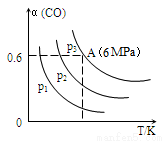
①p1、p2、p3中最大的是________。
②若該反應進行50min時達到平衡,此時CO的轉化率α=0.6,則50min內H2的反應速率為____mol·L-1·min-1。
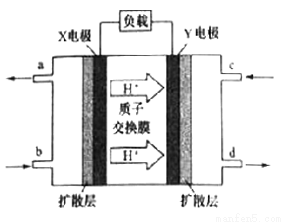
(3)二甲醚(CH3OCH3)燃料電池具有啟動快。效率高等優點,其能量密度高于甲醇燃料電池。其工作原理如圖所示。X極附近的酸性______(填“減弱”、“增強”或“不變”),Y電極是_____極,寫出X電極上發生的電極反應式__________。若用該二甲醚燃料電池電解飽和食鹽水(陽極為石墨電極),當有2.3g燃料被消耗時,陰極產生氣體的體積為_____L(標準狀況下)
查看答案和解析>>
科目:高中化學 來源:遼寧省大連市2017屆高三3月雙基測試化學試卷 題型:選擇題
能正確表示下列反應的離子方程式是
A. 用石墨作電極電解CuCl2溶液:2Cl-+2H2O 2OH-+Cl2↑+H2↑
2OH-+Cl2↑+H2↑
B. 0.01mol/LNH4Al(SO4)2溶液與0.02mol/LBa(OH)2溶液等體積混合:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
C. 將少量二氧化硫通入次氯酸鈉溶液:SO2+ClO-+2OH-=SO42-+Cl-+H2O
D. Ca(HCO3)2溶液與過量NaOH溶液反應:Ca2++HCO3-+OH-=CaCO3+H2O
查看答案和解析>>
科目:高中化學 來源:2017屆重慶市高三下學期第一次月考理科綜合化學試卷(解析版) 題型:簡答題
工業上“中溫焙燒——鈉化氧化法”回收電鍍污泥中的鉻已獲技術上的突破。其工藝流程如下:
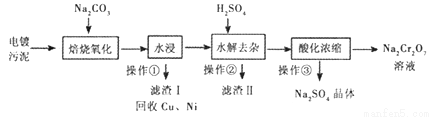
【查閱資料】
①電鍍污泥中含有Cr(OH)3、Al203、ZnO、CuO、NiO等物質;水浸后溶液中含有Na2CrO4、NaAlO2、Na2ZnO2等物質;
②Na2CrO4轉化成Na2Cr2O7離子反應方程式為:2 CrO42-+2H+=Cr2O72-+H2O;③Na2SO4、Na2Cr2O7、Na2CrO4在不同溫度下的溶解度如下表:

請回答:
(1)操作①的名稱是_______,“水浸”后的溶液呈_______性;
(2)“焙燒氧化”過程中Cr(OH)3轉化成Na2CrO4的化學方程式為___________;
(3)濾渣II的主要成分有Zn(OH)2和X,生成X的離子反應方程式__________;
(4)“酸化濃縮”時,需繼續加入H2SO4,然后_______、結晶、過濾。繼續加入H2SO4目的是__________;
(5)以鉻酸鈉為原料,電化學法制備重鉻酸鈉的實驗裝置如圖所示。
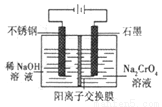
①陰極發生的電極反應式為:_____________;
②若測定陽極液中Na與Cr的物質的量之比值為d,則此時鉻酸鈉的轉化率為___________。
查看答案和解析>>
科目:高中化學 來源:2017屆貴州省貴陽市高三2月適應性考試(一)理綜化學試卷(解析版) 題型:推斷題
有機物G(分子式為C16H22O4)是常用的皮革、化工、油漆等合成材料中的軟化劑,它的一種合成路線如下圖所示:
已知:① A是一種常見的烴的含氧衍生物,A的質譜圖中最大質荷比為46,其核磁共振氫譜圖中有三組峰,且峰面積之比為1:2:3;
② E是苯的同系物,相對分子質量在10~110之間,且E苯環上的一氯代物只有2種;
③ 1molF與足量的飽和NaHCO3溶液反應可產生氣體44.8L(標準狀況下);
④ (R1、R2表示氫原子或烴基)。
(R1、R2表示氫原子或烴基)。
請根據以上信息回答下列問題:
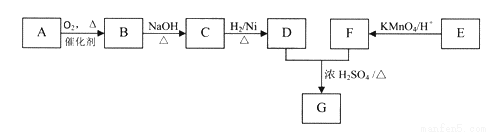
(1)A的名稱為_______;請寫出A 的一種同分異構體的結構簡式_________;
(2)A轉化為B的化學方程式為__________________________;
(3)C中所含官能團的名稱為_________;
(4)E的結構簡式為______________;
(5)D和F反應生成G的化學反應方程式為______________________;
(6)F有多種同分異構體,寫出同時滿足下列條件的F的同分異構體的結構簡式_____(填寫兩種即可)。
① 能和NaHCO3溶液反應;② 能發生銀鏡反應;③ 遇FeC13溶液顯紫色。
(7)參照上述流程信息和己知信息,設計以乙醇和丙醇為原料(無機試劑任選)制備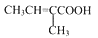 的合成路線_______________。合成路線流程圖示例如下:
的合成路線_______________。合成路線流程圖示例如下: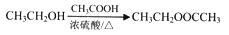
查看答案和解析>>
科目:高中化學 來源:2017屆貴州省貴陽市高三2月適應性考試(一)理綜化學試卷(解析版) 題型:選擇題
鋰一二硫化亞鐵電池是一種高容量電池,用途廣泛,該電池放電時的總反應為:4Li+FeS2=Fe+2Li2S。下列說法正確的是
A. 放電時,負極反應為:Li-e-=Li+
B. 放電時,正極發生氧化反應
C. 硫酸、羧酸及醇類物質都可以用作該鋰電池的電解質
D. 充電時,陽極只有Fe參與放電
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南省長沙市高二上學期期末考試化學試卷(解析版) 題型:推斷題
已知:醛(或酮)在一定條件下(稀NaOH溶液中)可以兩分子加成得到β-羥基醛(或酮),后者微熱脫水生成α、β不飽和醛(或酮)。
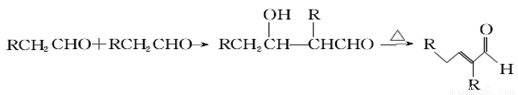
聚合物F的合成路線圖如下:
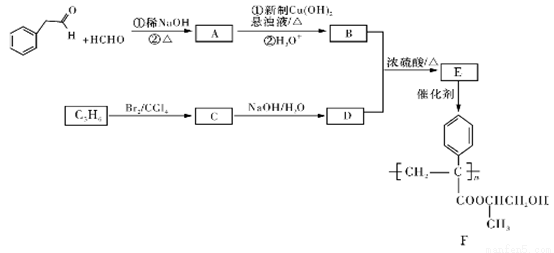
請據此回答:
(1)A中含氧官能團名稱是_________。
(2)E→F的反應類型是____________。
(3)寫出下列反應的化學方程式:
A→B的反應①__________________________;
C→D:____________________________;
(4)已知同一個碳原子上連兩個碳碳雙鍵的結構不穩定,如果C與NaOH的醇溶液反應,則生成的有機物的結構簡式為_______________。
(5)G物質與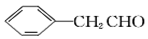 互為同系物,且G物質的相對分子質量比
互為同系物,且G物質的相對分子質量比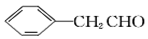 大14,則符合下列條件的G的同分異構體有________種。
大14,則符合下列條件的G的同分異構體有________種。
① 分子中含有苯環,且苯環上有兩個取代基
② 遇氯化鐵溶液變紫色
③ 能與溴水發生加成反應
(6)參照上述合成路線,設計一條由甲醛、丙醛和甲醇為有機原料(除溶劑外不得使用其它有機物)合成有機玻璃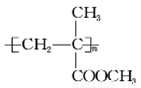 的合成路線。____________
的合成路線。____________
查看答案和解析>>
科目:高中化學 來源:2016-2017學年浙江省臺州市高一上學期期末質量評估考試化學試卷(解析版) 題型:填空題
A、B、C均為中學化學常見的純凈物,它們之間存在如下轉化關系,其中①②③均為有單質參與的反應。
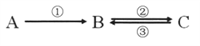
(1)若A是常見的金屬,①③中均有同一種氣態非金屬單質參與反應,B溶液遇KSCN顯血紅色,且②為化合反應,寫出反應②的離子方程式________。
(2)若B是太陽能電池用的光伏材料,①②③為工業制備B的反應。C的化學式是______,寫出反應①的化學方程式___________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com