
| A. | 含MnO2的分散系中,K+、H2O2、S、Br--可以大量共存 | |
| B. | MnO2和濃鹽酸反應的離子方程式:4HCl+MnO2═2Cl-+Cl2↑+Mn2++2H2O | |
| C. | MnO2在高錳酸鉀的分解反應中是氧化產物 | |
| D. | 1 mol MnO2和參與反應:3MnO2+4Al═3Mn+2Al2O3,轉移4 mol電子 |
分析 A.雙氧水在二氧化錳作催化劑時會分解生成氧氣,雙氧水能夠氧化硫離子、溴離子;
B.濃鹽酸在離子方程式中應該拆開,且需要加熱條件下才能反應;
C.高錳酸鉀中Mn元素的化合價為+7,二氧化錳中Mn元素為+4價,根據化合價變化判斷;
D.3mol二氧化錳完全反應轉移了12mol電子,據此進行計算.
解答 解:A.H2O2與S2-、Br-之間發生氧化還原反應,在二氧化錳作催化劑條件下,雙氧水會分解,在溶液中不能大量共存,故A錯誤;
B.MnO2和濃鹽酸反應中,需要加熱,且氯化氫應該拆開,正確的離子方程式為:2Cl-+4H++MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O,故B錯誤;
C.高錳酸鉀中Mn元素的化合價為+7,MnO2中Mn元素為+4價,該反應中Mn元素的化合價降低被還原,二氧化錳為還原產物,故C錯誤;
D.反應3MnO2+4Al═3Mn+2Al2O3中,3mol二氧化錳完全反應轉移了12mol電子,則1mol二氧化錳完全反應轉移4mol電子,故D正確;
故選D.
點評 本題考查了氧化還原反應的判斷,題目難度中等,明確氧化還原反應的實質及氧化產物、還原產物的概念為解答關鍵,試題培養了學生的靈活應用能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 可能呈酸性 | B. | 可能呈中性 | C. | 一定呈堿性 | D. | 一定呈中性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 16g CH4中含有4NA個C-H鍵 | |
| B. | 一定條件下,氨與氧氣在催化劑作用下反應生成30g NO,轉移電子數為5NA個 | |
| C. | 常溫常壓下,13.8g NO2與水充分反應,產生0.1N A個NO分子 | |
| D. | 標準狀況下,22.4 LCCl4中含有N A個CCl4分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 11:1 | B. | 9:2 | C. | 1:11 | D. | 2:9 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 化學反應 | 焓變 | 平衡常數 | 溫度/℃ | ||
| 500 | 700 | 800 | |||
| ①2H2(g)+CO(g)?CH3OH(g) | △H1 | K1 | 2.5 | 0.34 | 0.15 |
| ②CO2(g)+H2(g)?CO(g)+H2(g) | △H2 | K2 | 1.0 | 1.70 | 2.52 |
| ③CO2(g)+3H2(g)?CH3OH(g)+H2(g) | △H3 | K3 | |||
| 容器 | 甲 | 乙 | 丙 | |
| 反應物投入量 | 1molCO 2mol H2 | 1mol CH3OH | 2mol CH3OH | |
| 平衡時數據 | CH3OH的濃度(mol/L) | C1 | C2 | C3 |
| 反應體系的能量變化 | aKJ | bKJ | cKJ | |
| 體系壓強(Pa) | P1 | P2 | P3 | |
| 反應物轉化率 | a1 | a2 | a3 | |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ag+>Cu2+>Fe2+ | B. | Cu2+>Ag+>Fe2+ | C. | Ag+>Fe2+>Cu2+ | D. | Fe2+>Cu2+>Ag+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
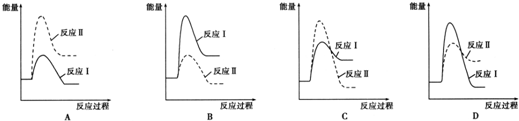
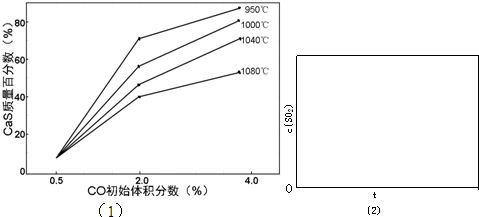
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com