
| 溶質 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.1 | 8.8 | 11.6 | 10.3 | 11.1 | 11.3 |
分析 (1)六種鹽都為強堿弱酸鹽,鹽的pH越大,說明對應的酸水解程度越大,則對應的酸越弱,根據強酸生成弱酸的特點判斷反應能否進行;
(2)先判斷過量,然后計算出混合液中氯離子的濃度,最后根據氯化銀溶度積常數進行計算c(Ag+).
解答 解:(1)六種鹽都為強堿弱酸鹽,鹽的pH越大,說明對應的酸水解程度越大,則對應的酸越弱,
A.CH3COOH酸性大于HCN,反應CH3COOH+NaCN═CH3COONa+HCN能發生,故A正確;
B.酸性H2CO3>HClO>HCO3-,應生成NaHCO3,反應CO2+H2O+2NaClO═Na2CO3+2HClO不能發生,故B錯誤;
C.酸性C6H5OH>HCO3-,反應Na2CO3+C6H5OH→NaHCO3+C6H5ONa能發生,故C正確;
D.酸性H2CO3>C6H5OH>HCO3-,反應生成碳酸氫鈉,正確反應為CO2+H2O+C6H5ONa→NaHCO3+C6H5OH反,故D錯誤,
故答案為:BD;
(2)向50mL 0.018mol•L-1的AgNO3溶液中加入相同體積0.020mol•L-1的鹽酸,鹽酸過量,反應后的c(Cl-)=$\frac{0.022mol/L×0.05L-0.018mol/L×0.05L}{0.1L}$=0.002mol/L,
則:c(Ag+)=$\frac{1.8×1{0}^{-10}}{0.002}$mol/L=9×10-8mol/L,
故答案為:9.0×10-8 mol/L.
點評 本題考查了酸性強弱與電離平衡常數的關系及難溶物溶度積的計算,題目難度中等,明確酸性強弱與電離平衡常數的關系為解答關鍵,注意掌握難溶物溶度積的表達式及計算方法,試題培養了學生的靈活應用能力.


 靈星計算小達人系列答案
靈星計算小達人系列答案 孟建平錯題本系列答案
孟建平錯題本系列答案科目:高中化學 來源: 題型:解答題
| 測定時間/小時鐘 | 0 | 1 | 2 | 4 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 該反應的熱化學方程式為:N2+3H2?2NH3△H=-92KJ/mol | |
| B. | a曲線是加人催化劑時的能量變化曲線 | |
| C. | 加人催化劑,該化學反應的放熱減少 | |
| D. | 反應物的總能量高于生成物的總能量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溶液中n(Fe2+)與n(Fe3+)之比為6:1 | |
| B. | 氧化產物與還原產物的物質的量之比為2:5 | |
| C. | 鐵有剩余,溶液呈淺綠色,c(Cl-)基本不變 | |
| D. | 往溶液中滴加無色KSCN溶液,不變色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2000kJ | B. | △H=-2000kJ/mol | C. | △H=-1500kJ/mol | D. | -2000kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=14的溶液中:CO32-、Na+、S2-、AlO2- | |
| B. | 室溫下水電離的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ | |
| C. | 室溫下$\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:Fe2+、Al3+、NO3-、I- | |
| D. | 無色溶液中:Al3+、NH4+、Cl?、HCO3? |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將金屬A投入B的鹽溶液,A溶解說明A的金屬性比B的金屬性強 | |
| B. | 氯堿工業和金屬鈉的冶煉都用到了NaC1,在電解時它們的陰極都是Na+得電子 | |
| C. | 向硫酸溶液中加入適量氨水,當溶液中c(SO42-)=c(NH4+)時,溶液呈酸性 | |
| D. | 等物質的量濃度的下列溶液中①NH4Cl ②NH4Al(SO4)2 ③NH3•H2O ④CH3COONH4,c(NH4+)由大到小的順序是:①>②>③>④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
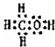 .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com