
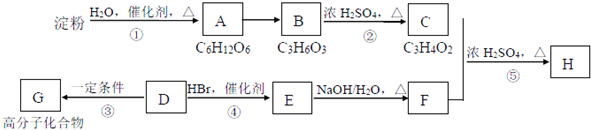
 ;反應類型:加聚反應.反應④的化學方程式:CH3CH=CH2+HBr$\stackrel{催化劑}{→}$CH3CHBrCH3;反應類型:加成反應.
;反應類型:加聚反應.反應④的化學方程式:CH3CH=CH2+HBr$\stackrel{催化劑}{→}$CH3CHBrCH3;反應類型:加成反應.分析 烴D的相對分子質量為42,則其含C原子個數為$\frac{42}{12}$=3---6,說明其分子式為C3H6,D是石油裂解氣的主要成分,應為丙烯CH3CH=CH2,丙烯與HBr發生加成反應生成的E分子中只有兩種類型的氫,則E為CH3CHBrCH3,E在NaOH的水溶液中水解生成醇F為CH3CHOHCH3,D在一定條件下生成高分子化合物G是丙烯的加聚反應,反應方程式為 ,淀粉水解生成的A為葡萄糖,葡萄糖水解生成乳酸
,淀粉水解生成的A為葡萄糖,葡萄糖水解生成乳酸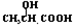 ,C 能使溴的四氯化碳溶液褪色,說明乳酸發生消去反應生成的C為CH2=CHCOOH,其與CH3CHOHCH3通過酯化反應生成H,據此分析.
,C 能使溴的四氯化碳溶液褪色,說明乳酸發生消去反應生成的C為CH2=CHCOOH,其與CH3CHOHCH3通過酯化反應生成H,據此分析.
解答 解:烴D的相對分子質量為42,則其含C原子個數為$\frac{42}{12}$=3---6,說明其分子式為C3H6,D是石油裂解氣的主要成分,應為丙烯CH3CH=CH2,丙烯與HBr發生加成反應生成的E分子中只有兩種類型的氫,則E為CH3CHBrCH3,E在NaOH的水溶液中水解生成醇F為CH3CHOHCH3,D在一定條件下生成高分子化合物G是丙烯的加聚反應,反應方程式為 ,淀粉水解生成的A為葡萄糖,葡萄糖水解生成乳酸
,淀粉水解生成的A為葡萄糖,葡萄糖水解生成乳酸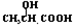 ,C 能使溴的四氯化碳溶液褪色,說明乳酸發生消去反應生成的C為CH2=CHCOOH,其與CH3CHOHCH3通過酯化反應生成H,
,C 能使溴的四氯化碳溶液褪色,說明乳酸發生消去反應生成的C為CH2=CHCOOH,其與CH3CHOHCH3通過酯化反應生成H,
(1)淀粉是多糖,淀粉水解生成的A為葡萄糖,葡萄糖是多羥基醛,結構簡式為CH2OH(CHOH)4CHO,故答案為:多;CH2OH(CHOH)4CHO;
(2)C 能使溴的四氯化碳溶液褪色,說明乳酸發生消去反應生成的C為CH2=CHCOOH,其含有碳碳雙鍵和羧基;CH2=CHCOOH與CH3CHOHCH3通過酯化反應生成H,H的結構簡式為CH2=CHCOOCH(CH3)2,故答案為:碳碳雙鍵和羧基;CH2=CHCOOCH(CH3)2;
(3)淀粉水解生成葡萄糖的化學方程式為:(C6H10O5)n+n H2O$\stackrel{催化劑}{→}$n C6H12O6,D在一定條件下生成高分子化合物G是丙烯的加聚反應,反應方程式為 ,丙烯與HBr發生加成反應生成的E分子中只有兩種類型的氫,則E為CH3CHBrCH3,化學方程式為CH3CH=CH2+HBr$\stackrel{催化劑}{→}$CH3CHBrCH3,
,丙烯與HBr發生加成反應生成的E分子中只有兩種類型的氫,則E為CH3CHBrCH3,化學方程式為CH3CH=CH2+HBr$\stackrel{催化劑}{→}$CH3CHBrCH3,
故答案為:(C6H10O5)n+n H2O$\stackrel{催化劑}{→}$n C6H12O6; ;加聚反應;CH3CH=CH2+HBr$\stackrel{催化劑}{→}$CH3CHBrCH3;加成反應;
;加聚反應;CH3CH=CH2+HBr$\stackrel{催化劑}{→}$CH3CHBrCH3;加成反應;
(4)B為乳酸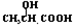 ,其可能的同分異構體有CH2OHCH2COOH,CH2OHCHOHCHO,故答案為:CH2OHCH2COOH;CH2OHCHOHCHO.
,其可能的同分異構體有CH2OHCH2COOH,CH2OHCHOHCHO,故答案為:CH2OHCH2COOH;CH2OHCHOHCHO.
點評 本題考查有機物推斷、烯與氯代烴、醇之間的轉化關系以及酯化反應等,難度不大,注意基礎知識的理解掌握.


 名校名師培優作業本加核心試卷系列答案
名校名師培優作業本加核心試卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化學 來源: 題型:解答題
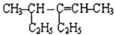 4-甲基-3-乙基-2-己烯
4-甲基-3-乙基-2-己烯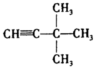 3,3-二甲基-1-丁炔.
3,3-二甲基-1-丁炔.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
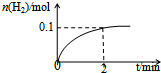 化學平衡:
化學平衡:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
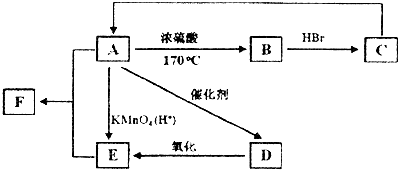
 ,
,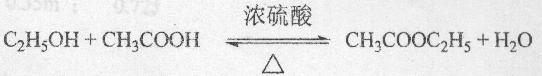 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題


 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$ +NaCl+H2O(注明反應條件).
+NaCl+H2O(注明反應條件).

 .
. .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 有機物A的結構簡式為
有機物A的結構簡式為 ,它可通過不同化學反應分別制得B、C和D三種物質.
,它可通過不同化學反應分別制得B、C和D三種物質. .
. +Br2→
+Br2→ .
.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 同溫同壓下,相同體積的物質,其物質的量一定相等 | |
| B. | 任何條件下,等物質的量的CO和NO所含的分子數一定相等 | |
| C. | 1L CO氣體一定比1L O2的質量小 | |
| D. | 相同條件下的CO和N2,若體積相等,則質量一定相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com