
| A. | 10 L 0.05mol•L-1Ba(OH)2溶液與10 L 0.05mol•L-1 H2SO4反應時的反應熱是中和熱 | |
| B. | 由2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ•mol-1知,該反應的反應熱為571.6 kJ•mol-1 | |
| C. | 由2H2(l)+O2(l)=2H2O(g)△H=-482.6 kJ•mol-1知,H2的燃燒熱為482.6 kJ•mol-1 | |
| D. | 由C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2221.5 kJ•mol-1知,氣體C3H8的燃燒熱為2221.5 kJ•mol-1 |
分析 A、生成沉淀一般還要放熱;
B、反應熱有符合;
C、燃燒熱是指氫氣燃燒生成液態水時放出的熱量;
D、燃燒熱為完全燃燒1mol丙烷生成二氧化碳和液態水時會放出的熱量.
解答 解:A.10 L 0.05 mol•L-1Ba(OH)2溶液與10 L 0.05mol•L-1 H2SO4反應時生成1mol水同時生成硫酸鋇沉淀,所以放出的熱量大于中和熱,故A錯誤;
B.反應熱有符合,所以由2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ•mol-1知,該反應的反應熱為-571.6 kJ•mol-1,故B錯誤;
C.氫氣的燃燒熱是指生成液態水時放出的熱量,故C錯誤;
D.燃燒熱為完全燃燒1mol丙烷生成二氧化碳和液態水時會放出的熱量,所以由C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2221.5 kJ•mol-1知,氣體C3H8的燃燒熱為2221.5 kJ•mol-1,故D正確.
故選:D.
點評 本題主要考查了中和熱、燃燒熱的概念的理解,解題式應注意分析中和熱時①稀溶液②強酸強堿③生成1mol水,燃燒熱時①1mol燃料②生成穩定化合物,水難度不大.


 小學生10分鐘口算測試100分系列答案
小學生10分鐘口算測試100分系列答案科目:高中化學 來源: 題型:選擇題
| A. | 3 mol NF3與水完全反應生成HNO3和NO,轉移電子數為2NA | |
| B. | 4.4 g14CO2含中子數為2.4NA | |
| C. | 標準狀況下,2.24 L Cl2通入足量NaOH溶液中,反應轉移電子的數目為0.2NA | |
| D. | 常溫常壓下,1.7 g H2O2中含有的電子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③④ | B. | ③④⑤⑥ | C. | ⑤⑥ | D. | ②④⑤⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 7.2g CaO2晶體中陰離子和陽離子總數為0.3NA | |
| B. | 反應3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol放出熱量9.2kJ時,轉移電子0.6NA | |
| C. | 0.1mol/LNH4Cl溶液中Cl-離子數目為0.1NA | |
| D. | 0.1molH2O2分子中含極性共價鍵數目為0.3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
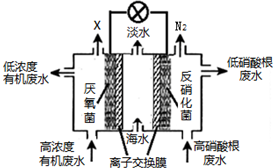
| A. | 中間室Cl-移向左室 | |
| B. | X氣體為CO2 | |
| C. | 處理后的含硝酸根廢水pH降低 | |
| D. | 電路中每通過4 mol電子,產生標準狀況下X的體積為22.4L |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 用標準鹽酸滴定待測氫氧化鈉溶液至終點,讀數時視線偏高 | |
| B. | 用含Na2O的NaOH固體配制成的標準溶液,滴定待測鹽酸 | |
| C. | 將4.0g NaOH溶解后迅速轉移入1L的容量瓶中定容,配制0.1moL/L的NaOH溶液 | |
| D. | 將1mL 98%的濃硫酸加入9mL水中,配制9.8%的稀硫酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 實驗室制氯氣:MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| B. | 實驗室制二氧化硫:Cu+SO42-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Cu2++SO2↑+2H20 | |
| C. | 實驗室用濃氨水與生石灰制氨氣:NH3•H20═Ca(OH)2+NH3↑ | |
| D. | 實驗室制二氧化氮:Cu+4H++2NO3-═Cu2++2NO2↑+2H20 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| X | Z | |
| Y |
| A. | 原子序數由大到小為 Z>Y>X | |
| B. | 氫化物最穩定的元素為Y | |
| C. | X的最高價氧化物對應的水化物的稀溶液能與銅發生反應 | |
| D. | 原子半徑由大到小的順序為 Z>Y>X |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com