
| A. | 用鐵片和稀硫酸反應制取氫氣時,改用98%的濃硫酸可以加快產生氫氣的速率 | |
| B. | 100mL 2mol/L的鹽酸跟鋅片反應,加入適量的氯化鈉溶液,反應速率不變 | |
| C. | SO2的催化氧化是一個放熱的反應,所以升高溫度,反應的速率減慢 | |
| D. | 在其他條件不變時,使用催化劑只能改變反應速率,而不能改變化學平衡狀態 |
分析 A.濃硫酸與鐵反應發生鈍化反應;
B.加入氯化鈉,溶液體積增大,濃度減小;
C.升高溫度,增大反應速率;
D.催化劑同等程度改變反應速率.
解答 解:A.常溫下濃硫酸與鐵反應發生鈍化反應,如加熱,則生成二氧化硫氣體,不能增大生成氫氣的速率,故A錯誤;
B.加入氯化鈉,氯化鈉不參與反應,但溶液體積增大,濃度減小,速率減小,故B錯誤;
C.升高溫度,增大活化分子百分數,增大反應速率,故C錯誤;
D.催化劑同等程度改變反應速率,平衡不移動,故D正確.
故選D.
點評 本題考查化學反應速率的影響因素,為高頻考點,側重學生的分析能力的考查,注意把握影響化學反應速率的因素以及相關物質的性質,難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 6種 | B. | 4種 | C. | 2種 | D. | 1種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,1L0.1mol•L-1氫氟酸溶液中含有的H+離子數為0.1NA | |
| B. | 密閉容器中,2molSO2與4molO2充分反應轉移的電子數為4NA | |
| C. | 25℃時,pH=13的Na2CO3溶液中含有的OH-兩種數為NA | |
| D. | 常溫下,1L1mol•L-1NaOH溶液中含有的陽離子總數大于NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO和N2 | B. | O3和SO2 | C. | CO2和N2O | D. | N2H4和C2H4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④ | B. | ①② | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 把少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═2HClO+CaSO3↓ | |
| B. | 足量鐵屑溶于稀硫酸:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 碳酸氫鈣溶液中加入足量燒堿溶液:HCO3-+OH-═CO32-+H2O | |
| D. | 鋁片溶于燒堿溶液:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 元素編號 | 元素性質或原子結構 |
| T | 最外層電子數是次外層電子數的2倍 |
| X | L層有三個未成對電子 |
| Y | L層p電子數比s電子數多兩個 |
| Z | 元素的最高正價為+7價 |
| A. | z離子的結構示意圖為: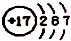 | B. | 分子TY2的鍵角為l80° | ||
| C. | X原子的軌道式為: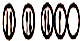 | D. | XZ3為非極性分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分液時,分液漏斗下層液體從下端放出,上層液體從上口倒出 | |
| B. | 蒸餾時,應使溫度計水銀球靠近蒸餾燒瓶支管口 | |
| C. | 蒸發結晶時應將溶液直接蒸干 | |
| D. | 稱量非腐蝕性藥品應放在托盤天平左盤的稱量紙上,砝碼放在托盤天平右盤的稱量紙上 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com