

分析 待處理鍍銅電路板與氯化鐵溶液反應后得到的溶液中含有氯化銅、氯化亞鐵及未反應的氯化鐵,廢液中加入足量的Fe,反應中鐵離子和銅離子均可鐵粉反應:2Fe3++Fe═3Fe2+,Cu2++Fe=Cu+Fe2+,過濾得到的固體1為生成的銅和過量的鐵,加入適量鹽酸后過濾,Fe與鹽酸反應,而Cu不反應,過濾得到固體2為銅及氯化亞鐵溶液,新制氯水把氯化亞鐵氧化,得到氯化鐵溶液.(2)中檢驗溶液中Fe3+存在通常用KSCN溶液,溶液變紅說明Fe3+存在,據此解答.
解答 解:待處理鍍銅電路板與氯化鐵溶液反應后得到的溶液中含有氯化銅、氯化亞鐵及未反應的氯化鐵,廢液中加入足量的Fe,反應中鐵離子和銅離子均可鐵粉反應:2Fe3++Fe═3Fe2+,Cu2++Fe=Cu+Fe2+,過濾得到的固體1為生成的銅和過量的鐵,加入適量鹽酸后過濾,Fe與鹽酸反應,而Cu不反應,過濾得到固體2為銅及氯化亞鐵溶液,新制氯水把氯化亞鐵氧化,得到氯化鐵溶液.
(1)鍍銅電路版制成印刷電路版是利用氯化鐵溶液和銅反應生成氯化亞鐵和氯化銅而實現的,離子方程式為2Fe3++Cu═Cu2++2Fe2+,廢液中含有鐵離子和銅離子均可以與過量鐵粉反應,濾得到的固體1為生成的銅和過量的鐵,
故答案為:2Fe3++Cu═Cu2++2Fe2+; Fe、Cu;
(2)反應①為銅與氯化鐵溶液反應生成氯化亞鐵和氯化鐵,化學方程式為:2FeCl3+Cu=2FeCl2+CuCl2,檢驗溶液中Fe3+存在通常用KSCN溶液,取少量溶液與試管中,滴加KSCN溶液,溶液變紅說明Fe3+存在,
故答案為:2FeCl3+Cu=2FeCl2+CuCl2;KSCN;
(3)反應④是新制氯水把氯化亞鐵氧化為三氯化鐵,反應的離子方程式為:2Fe2++Cl2=2Fe3++2Cl-,故答案為:2Fe2++Cl2=2Fe3++2Cl-.
點評 本題考查化學工藝流程、物質分離提純綜合應用、元素化合物性質等知識,側重于鐵離子和亞鐵離子的轉化,題目難度中等,注意基礎知識的理解掌握.


科目:高中化學 來源: 題型:多選題
| A. | 將木炭粉碎成粉末狀可以加快化學反應速率 | |
| B. | 升高溫度可以加快化學反應速率 | |
| C. | 增加壓強可以加快化學反應速率 | |
| D. | 增加木炭的量可以加快化學反應速 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
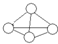 白磷分子如圖所示,則31g白磷分子中存在的共價鍵數目是( )
白磷分子如圖所示,則31g白磷分子中存在的共價鍵數目是( )| A. | 4NA | B. | NA | C. | 1.5NA | D. | 0.25NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 鐵在冷的濃硫酸中能發生鈍化.某興趣小組的同學發現將鐵與一定量的濃硫酸加熱時,觀察到鐵完全溶解得到溶液A,并產生大量氣體B.
鐵在冷的濃硫酸中能發生鈍化.某興趣小組的同學發現將鐵與一定量的濃硫酸加熱時,觀察到鐵完全溶解得到溶液A,并產生大量氣體B.| 實驗操作 | 預期現象 | 結 論 | |
| 驗證猜想Ⅰ | ①取適量A溶液,滴加0.1mol/LKSCN溶液 ②另取適量A溶液,滴加少量0.01mol/L酸性KMnO4溶液 | ①酸性高錳酸鉀溶液褪色,說明含有亞鐵離子; ②溶液變為血紅色 | 含有Fe2+和Fe3+ |
| 驗證猜想Ⅱ | 將所得氣體通入下圖所示裝置 | 甲中紫色褪去,乙中不褪色,試管中收集到氣體 | 含有兩種氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 反應 | △H/kJ•mol-1 | △S/J•K-1•mol-1 |
| ① | -72.1 | +220 |
| ② | +149 | +41 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com