
【題目】已知NO2和N2O4可以相互轉化:反應2NO2(g)![]() N2O4(g)△H=﹣57.2kJ/mol。
N2O4(g)△H=﹣57.2kJ/mol。
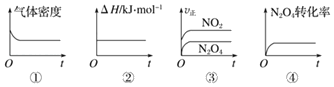
(1)一定溫度下,現將1molN2O4充入一恒壓密閉容器中,下列示意圖正確且能說明反應達到平衡狀態的是___(填序號,下同)。
(2)若反應2NO2(g)N2O4(g)在體積為1L的恒容密閉容器中進行,保持溫度不變,達到平衡后,向反應容器中再充入少量N2O4,平衡向___移動(填“左”、“右”或“不”),重新平衡后和原平衡相比,混合氣體顏色___(填“變深”“變淺”或“不變”),N2O4 的體積分數___(填“增大”、“減小”或“不變”)。
(3)一定溫度下,向容積為20L的密閉容器中充入1molNO2氣體,發生反應2NO2(g)N2O4(g),反應中測得相關數據如表所示:
反應時間/min | 0 | 10 | 20 | 30 | 40 | 50 |
氣體相對分子質量 | 46 | 57 | 64 | 69 | 69 | 69 |
①此條件下該反應的化學平衡常數K=___。
②在50min末,向容器中加入![]() molNO2,若要保持平衡不發生移動,應加入N2O4為___mol。
molNO2,若要保持平衡不發生移動,應加入N2O4為___mol。
【答案】①④ 左 變深 增大 60 ![]()
【解析】
(1)未達到平衡狀態時體系中某些值是不斷變化的,當這些值不變時可說明反應達到平衡狀態;
(2)二氧化氮氣體為紅棕色,若二氧化氮濃度增大,則顏色加深;
(3)①平衡常數K=![]() ;
;
②濃度商等于平衡常數時平衡不發生移動;
(1)a.該反應是體積變化的反應,密閉容器中氣體質量不變,所以密度不變,說明達到了平衡狀態,故①正確;
b.反應熱△H與化學反應方程式有關,是不變化的,所以△H始終不變,不能判斷是否達到平衡狀態,故②錯誤;
c.根據正反應速率大小關系,無法判斷同一物質的正逆反應速率是否相等,故③錯誤;
d.四氧化二氮的轉化率不變,說明四氧化二氮的濃度不變,說明反應達到了平衡狀態,故④正確;
故答案為:①④;
(2)可逆反應為2NO2(g)N2O4(g),達到平衡后,向反應容器中再充入少量N2O4,生成物濃度增大,平衡向左移動,c(NO2)增大,混合氣體顏色變深,恒容密閉容器中體積不變時可看成增大壓強,壓強增大時平衡正向移動,導致N2O4的體積分數增大,故答案為:左;變深;增大;
(3)①反應2NO2(g)N2O4(g)的三段式為,
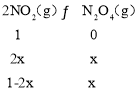
混合氣體的物質為46g,平衡時,混合氣體的相對分子質量為69,即69(1﹣2x+x)=46,x=![]() mol,c(NO2)=c(N2O4)=
mol,c(NO2)=c(N2O4)=![]() =
=![]() mol/L,
mol/L,
② 該反應的化學平衡常數K=![]() =
=![]() =60,故答案為:60;
=60,故答案為:60;
②設平衡時N2O4的濃度為c(N2O4),向容器中加入![]() molNO2,此時c(NO2)=
molNO2,此時c(NO2)=![]() =0.05mol/L,化學平衡常數K=
=0.05mol/L,化學平衡常數K=![]() =
=![]() =60,則c(N2O4)=0.15mol/L,n(N2O4)=cV=20L×0.15mol/L=3mol,所以應加入N2O4的物質的量為3mol﹣
=60,則c(N2O4)=0.15mol/L,n(N2O4)=cV=20L×0.15mol/L=3mol,所以應加入N2O4的物質的量為3mol﹣![]() mol=
mol=![]() mol,故答案為:
mol,故答案為:![]() 。
。


 高中必刷題系列答案
高中必刷題系列答案科目:高中化學 來源: 題型:
【題目】將一定量的X加入某密閉容器中,發生反應:2X(g)![]() 3Y(g)+Z(g),混合氣體中X的物質的量分數與溫度關系如圖所示:下列推斷正確的是()。
3Y(g)+Z(g),混合氣體中X的物質的量分數與溫度關系如圖所示:下列推斷正確的是()。
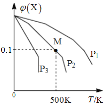
A. 升高溫度,該反應平衡常數K減小
B. 壓強大小有P3>P2>P1
C. 平衡后加入高效催化劑使平均摩爾質量增大
D. 在該條件下M點X平衡轉化率為9/11
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某鉛酸蓄電池的工作原理如圖所示,其總反應式為![]() 。下列判斷不正確的是
。下列判斷不正確的是

A.閉合K時,d電極的反應式為![]()
B.當電路中轉移![]() 電子時,Ⅰ中消耗的
電子時,Ⅰ中消耗的![]() 為
為![]()
C.閉合K時,Ⅱ中![]() 向c電極遷移
向c電極遷移
D.閉合K一段時間后,Ⅱ可單獨作為原電池,d電極為正極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列能用勒沙特列原理解釋的是
A. Fe(SCN)3溶液中加入固體KSCN后顏色變深
B. 棕紅色Br2蒸氣加壓后顏色變深
C. SO2催化氧化成SO3的反應,往往需要使用催化劑
D. H2、I2、HI平衡混和氣加壓后顏色變深
查看答案和解析>>
科目:高中化學 來源: 題型:
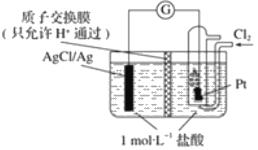
【題目】某原電池裝置如圖所示,電池總反應為 2Ag+Cl2═2AgCl。
(1)寫出該電池工作時的兩極反應:負極:___;正極:___。
(2)當電路中轉移amole﹣時,交換膜左側溶液中約減少___mol離子;交換膜右側溶液c(HCl)___(填“>”“<”或“=”)1molL-1(忽略溶液體積變化)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】FFC電解法可由金屬氧化物直接電解制備金屬單質,西北稀有金屬材料研究院利用此法成功電解制備鉭粉(Ta),其原理如圖所示。下列說法正確的是
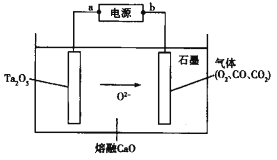
A. 該裝置將化學能轉化為電能
B. a極為電源的正極
C. Ta2O5極發生的電極反應為Ta2O5+10e—=2Ta+5O2—
D. 石墨電極上生成22.4 L O2,則電路中轉移的電子數為4×6.02×1023
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與社會生活密切相關,下列說法正確的是( )
A.軍艦船底鑲嵌鋅塊作正極,以防船體被腐蝕
B.汽車尾氣中NO和CO可以緩慢反應生成N2和CO2,減小壓強,反應速率減慢
C.金屬冶煉過程是金屬離子得電子變成金屬單質的氧化過程
D.PM2.5顆粒![]() 微粒直徑約為2.5×106m)分散在空氣中形成氣溶膠
微粒直徑約為2.5×106m)分散在空氣中形成氣溶膠
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列圖示與對應敘述相符的是
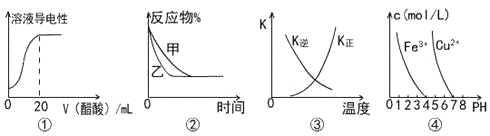
A.圖①表示向20 mL 0.1 mol/L氨水中逐滴加入0.1 mol/L醋酸,溶液導電性隨加入酸體積的變化
B.圖②表示壓強對可逆反應A(g)+2B(g)![]() 3C(g)+D(s)的影響,乙的壓強比甲的壓強大
3C(g)+D(s)的影響,乙的壓強比甲的壓強大
C.圖③中曲線表示反應3A(g) + B(g)![]() 2C(g)△H<0,正、逆反應的平衡常數K隨溫度的變化
2C(g)△H<0,正、逆反應的平衡常數K隨溫度的變化
D.據圖④,若要除去CuSO4溶液中的Fe3+,可加入NaOH溶液至pH在4左右
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在常溫下,有下列五種溶液:A.0.1mol/LNH4Cl B.0.1mol/L CH3COONH4 C.0.1mol/LNH4HSO4 D.0.1mol/LNH4HCO3 E.0.1mol/LNaHCO3
請根據要求填寫下列空白:
(1)溶液A呈___性(填“酸”、“堿”或“中”),其原因是:___(用離子方程式表示)。
(2)溶液E呈___性(填“酸”、“堿”或“中”),其原因是:___(用離子方程式表示)。
(3)比較溶液A、C中c(NH4+)的大小關系是A___C(填“>”、“<”或“=”)。
(4)常溫下,測得溶液B的pH=![]() ,則CH3COO-的水解程度___NH4+的水解程度(填“>”、“<”或“=”),CH3COO-與NH4+濃度的大小關系是:c(CH3COO-)___c(NH4+)(填“>”、“<”或“=”)。
,則CH3COO-的水解程度___NH4+的水解程度(填“>”、“<”或“=”),CH3COO-與NH4+濃度的大小關系是:c(CH3COO-)___c(NH4+)(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com