
| 實驗 序號 | 試劑體積 V/mL | 顯色時間 t/s | ||||
| K2S2O8溶液 | KI溶液 | 水 | Na2S2O3溶液 | 淀粉溶液 | ||
| ① | 10 | 10 | 0 | 4 | 1 | 26.8 |
| ② | 5 | 10 | 5 | 4 | 1 | 54.0 |
| ③ | 2.5 | 10 | V1 | 4 | 1 | 108.2 |
| ④ | 10 | 5 | 5 | 4 | 1 | 53.8 |
| ⑤ | 5 | 7.5 | 7.5 | 4 | V2 | t1 |
分析 (1)慢反應中有I2生成,使溶液變藍色,而快反應中消耗I2,慢反應決定反應速率,慢反應中生成I2大于快反應中消耗的I2,可以觀察到溶液變藍色;
(2)如果實驗中不使用Na2S2O3溶液,顯色時間會太短不易測量;
(3)實驗目的是探究反應物濃度對化學反應速率的影響,由表中①②③數據可知,KI溶液、Na2S2O3溶液用量相等,應是探究K2S2O8濃度對反應速率的影響,保持溶液總體積相等;②⑤中K2S2O8、Na2S2O3溶液用量相等,應是探究KI溶液濃度對反應速率的影響,保持其他條件一致;由①②實驗可知反應速率與反應物濃度成正比關系,與顯色時間成反比關系;
(4)由表中數據可知:反應物濃度越大,反應速率越快.
解答 解:(1)慢反應中有I2生成,使溶液變藍色,而快反應中消耗I2,慢反應決定反應速率,當溶液中的 S2O32-或Na2S2O3耗盡后,碘才能與淀粉作用顯示藍色,根據I2+2S2O32-═S4O62-+2I- (快)可知,1mol碘需2molS2O32-,根據方程式S2O82-+2I-═2SO42-+I2可知,生成1mol碘需為1molS2O82-,為確保能觀察到藍色,碘需有剩余,即n(S2O82-):n(S2O32-)>1:2,
故答案為:1:2;
(2)如果實驗中不使用Na2S2O3溶液,反應S2O82-+2I-=2SO42-+I2產生的碘就會使淀粉顯藍色,時間太短不易測量,
故答案為:顯色時間太短,不易測量;
(3)實驗目的是探究反應物濃度對化學反應速率的影響,由表中數據可知,①②③KI溶液、Na2S2O3溶液用量相等,應是探究K2S2O8濃度對反應速率的影響,保持溶液總體積相等,溶液的總體積為25mL,即其他條件不變,只改變反應物K2S2O8濃度,從而才達到對照實驗目的,故V1=(25-2.5-10-4-1)mL=7.5mL;實驗②⑤中K2S2O8、Na2S2O3溶液用量相等,應是探究KI溶液濃度對反應速率的影響,淀粉的用量應保持一致,所以V2=1mL;由①②實驗可知反應速率與反應物濃度成正比關系,與顯色時間成反比關系,實驗②⑤中KI的濃度與顯色時間的關系式為:$\frac{10}{7.5}=\frac{{t}_{1}}{54}$,t1=72s,
故答案為:7.5;保證每次實驗溶液總體積相等;1;保證淀粉溶液的用量相同;72s;
(4)實驗①②③是其他條件一致,K2S2O8的濃度越大,反應速率越快(成正比關系),實驗①④、②⑤是其他條件一致,KI溶液的濃度越大,反應速率越快(成正比關系),由此可知:反應速率與反應物濃度成正比關系(反應物濃度越大,反應速率越快),
故答案為:反應速率與反應物濃度成正比關系(反應物濃度越大,反應速率越快).
點評 本題考查化學反應速率影響因素的實驗探究,側重于學生的分析能力和實驗能力的考查,為高頻考點,控制變量法是解題的關鍵,考查學生靈活運用化學知識的能力,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | X只能位第三周期 | B. | Xn-一定有3個電子層 | ||
| C. | Y的原子序數不大于7 | D. | Y不可能位于第二周期 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該溶液中可能含有K+ | |
| B. | 該溶液中肯定含有NH4+、SO42-、AlO2-、NO3- | |
| C. | 該溶液中一定不含NO3- | |
| D. | 該溶液中一定含K+,且c(K+)≥0.1 mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 6.02×1023叫做阿伏加德羅常數 | |
| B. | 摩爾(mol)是國際單位制中七個基本單位之一 | |
| C. | 1mol氣體的體積隨壓強和溫度的增大而變小 | |
| D. | 氣體摩爾體積(Vm)是指1 mol任何氣體所占的體積都約為22.4 L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,5.6L二氧化碳氣體中含有的氧原子數為0.5NA | |
| B. | 0.1L0.5mol/LCH3COOH溶液中含有的氫離子數為0.05NA | |
| C. | 1molFe溶于過量硝酸,電子轉移數為2NA | |
| D. | 標準狀況下,2.24LCC14含有的共價鍵數為0.4NA |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
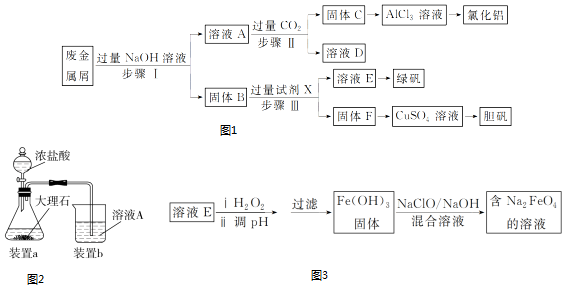
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com