
| A. | 元素原子的核外電子排布呈周期性變化 | |
| B. | 元素原子的最外層電子排布呈周期性變化 | |
| C. | 元素的化合價呈周期性變化 | |
| D. | 元素原子半徑呈周期性變化 |
分析 A、元素的性質由最外層電子決定;
B、隨原子序數的遞增,電子層數和最外層電子數都呈現周期性的變化而引起元素性質的周期性變化;
C、元素的最高正化合價的周期性變化是原子的電子排布周期性變化的結果;
D、元素的原子半徑的周期性變化是原子的電子排布周期性變化的結果.
解答 解:A、應由最外層電子的排布決定化學性質,故A錯誤;
B、由原子的電子排布可知,隨原子序數的遞增,電子層數和最外層電子數都呈現周期性的變化而引起元素性質的周期性變化,即原子的電子層排布的周期性變化是引起元素性質周期性變化的決定因素,故B正確;
C、化合價屬于元素的性質,元素的最高正化合價的周期性變化是原子的電子排布周期性變化的結果,故C錯誤;
D、元素的原子半徑屬于元素的性質,元素的原子半徑的周期性變化是電子排布周期性變化的結果,故D錯誤.
故選B.
點評 隨著原子序數的遞增,元素原子的核外電子排布的周期性變化導致元素性質(金屬性和非金屬性,原子半徑,化合價等)的周期性變化.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 正極反應式為KClO4(s)+8e?═KCl(s)+4O2?(l) | |
| B. | 在該熱電池中,鐵為負極,發生還原反應 | |
| C. | △H參與反應的高氯酸鉀越多,其值越小 | |
| D. | 生成1 mol FeO轉移8 mol電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 圖為制取純凈干燥的氣體A的裝置圖的一部分.生成A的速度可通過滴入液體B的速度控制.已知A是一種無色、無氣味的氣體,它不能使酸堿指示劑變色,也不能在空氣中燃燒,但能使帶火星的木條復燃.
圖為制取純凈干燥的氣體A的裝置圖的一部分.生成A的速度可通過滴入液體B的速度控制.已知A是一種無色、無氣味的氣體,它不能使酸堿指示劑變色,也不能在空氣中燃燒,但能使帶火星的木條復燃.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
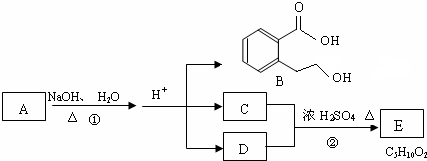
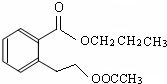 或
或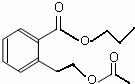 .
. .
.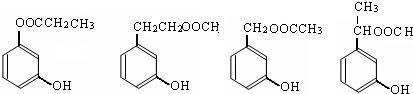 (寫出四者之一即可).
(寫出四者之一即可).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
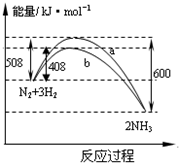
| A. | 該反應的熱化學方程式為:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)?NH3(g)△H=-92kJ•mol-1 | |
| B. | 曲線b表明加入催化劑降低了反應熱,加快了反應速率 | |
| C. | 加入催化劑,生成1molNH3的反應熱減小50KJ | |
| D. | 不用催化劑,生成1molNH3放出的熱量為46KJ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

| 物質 | SiCl4 | AlCl3 | FeCl3[來 | FeCl2 |
| 沸點/℃ | 57.6 | 180(升華) | 300(升華) | 1023 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com