
分析 (1)根據n=$\frac{m}{M}$計算氨氣物質的量,再根據N=nNA計算氨氣分子數目,氫原子為氨氣分子的3倍,根據V=nVm計算氨氣體積,含有電子物質的量為氨氣的10倍,根據c=$\frac{n}{V}$計算溶液物質的量濃度;
(2)計算二者物質的量,再根據總質量、總物質的量列方程計算CO和CO2的物質的量,根據V=nVm計算CO體積,根據m=nM計算CO質量;
(3)根據n=$\frac{m}{M}$計算Na2CO3•10H2O物質的量,碳酸鈉物質的量等于Na2CO3•10H2O的物質的量,根據c=$\frac{n}{V}$計算溶液物質的量濃度;
(4)體積之比等于物質的量之比,結合總質量計算各物質相應物質的量,再根據V=nVm計算氣體體積;
(5)根據n=$\frac{N}{{N}_{A}}$計算氣體物質的量,再根據M=$\frac{m}{n}$計算該氣體的摩爾質量;
(6)根據n=$\frac{V}{{V}_{m}}$計算HCl物質的量,根據m=nM計算HCl質量,溶液質量=水的質量+HCl質量,再根據V=$\frac{m}{ρ}$計算溶液體積,根據c=$\frac{n}{V}$計算溶液物質的量濃度.
解答 解:(1)氨氣物質的量為$\frac{3.4g}{17g/mol}$=0.2mol,氨氣分子數目為0.2mol×6.02×1023mol-1=1.204×1023,氫原子數目為3×1.204×1023=3.612×1023,標況下氨氣體積為0.2mol×22.4L/mol=4.48L,含有電子物質的量為0.2mol×10=2mol,溶液物質的量濃度為$\frac{0.2mol}{0.2L}$=1mol/L;
故答案為:1.204×1023;3.612×1023;4.48;2;1;
(2)CO和CO2混合氣體總物質的量為$\frac{22.4L}{22.4L/mol}$=1mol,設二者物質的量分別為xmol、ymol,則:$\left\{\begin{array}{l}{x+y=1}\\{28x+44y=36}\end{array}\right.$,解得x=y=0.5,故標況下CO體積為0.5mol×22.4L/mol=11.2L,CO質量為0.5mol×28gmol=14g,
故答案為:11.2;14;
(3)Na2CO3•10H2O物質的量=$\frac{1.43g}{286g/mol}$=0.005mol,碳酸鈉物質的量等于Na2CO3•10H2O的物質的量,溶液物質的量濃度為$\frac{0.005mol}{0.1L}$=0.05mol/L,
故答案為:0.05;
(4)同溫同壓下,體積比為1:2:3所組成的N2、O2和CO2的物質的量之比為1:2:3,設氮氣物質的量為n mol,則28n+2n×32+3n×44=33.6,解得n=0.15,故標況下混合氣體總體積為0.15mol×6×22.4L/mol=20.16L,
故答案為:20.16;
(5)該氣體物質的量為$\frac{6.02×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=1mol,該氣體的摩爾質量為$\frac{32g}{1mol}$=32g/mol,
故答案為:32g/mol;
(6)HCl物質的量為$\frac{aL}{22.4L/mol}$=$\frac{a}{22.4}$mol,HCl質量為$\frac{36.5a}{22.4}$g,溶液質量=(1000+$\frac{36.5a}{22.4}$)g,溶液體積=$\frac{(1000+\frac{36.5a}{22.4})g}{1000bg/L}$=$\frac{22400+36.5a}{22400b}$L,溶液物質的量濃度為$\frac{\frac{a}{22.4}mol}{\frac{22400+36.5a}{22400b}L}$=$\frac{1000ab}{22400+36.5a}$mol/L,
故答案為:$\frac{1000ab}{22400+36.5a}$mol/L.
點評 本題考查物質的量有關計算,難度不大,注意掌握以物質的量為中心的計算.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
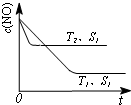 對大氣污染物SO2、NOx進行研究具有重要環保意義.請回答下列問題:
對大氣污染物SO2、NOx進行研究具有重要環保意義.請回答下列問題: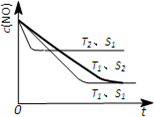 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
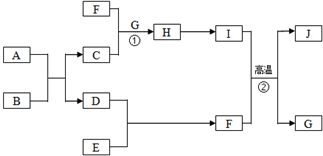 有關物質的轉化關系如圖所示(部分物質與條件已略去).A是常見的金屬單質,B是常見的強酸,E是空氣中含量最多的單質,I是既能與強酸又能與強堿反應的氧化物,G是最常見的無色液體,J是一種高硬度材料(摩爾質量為41g•mol-1).請回答下列問題:
有關物質的轉化關系如圖所示(部分物質與條件已略去).A是常見的金屬單質,B是常見的強酸,E是空氣中含量最多的單質,I是既能與強酸又能與強堿反應的氧化物,G是最常見的無色液體,J是一種高硬度材料(摩爾質量為41g•mol-1).請回答下列問題: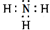 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | O2被還原 | |
| B. | 該反應是置換反應 | |
| C. | NH3是氧化劑 | |
| D. | 若有17gNH3參加反應,則反應中轉移的電子數為10 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 每生成6.72 L的H2,溶液中AlO2-的數目就增加0.2NA | |
| B. | 每生成0.15 molH2,被還原的水分子數目為0.3NA | |
| C. | 當加入2.7gAl時,轉移的電子數目為0.3NA | |
| D. | 溶液中每增加0.1mol的AlO2-,Na+的數目就增加0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
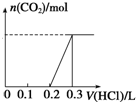 100mL 1mol•L-1燒堿溶液中通入一定量CO2充分反應后,將溶液在低溫下蒸干得到白色固體X,X的組成可能有四種情況,
100mL 1mol•L-1燒堿溶液中通入一定量CO2充分反應后,將溶液在低溫下蒸干得到白色固體X,X的組成可能有四種情況,查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1771年,法國科學家拉瓦錫發現元素周期律,把化學元素及其化合物納入一個統一的理論體系 | |
| B. | 化學科學與其他科學分支的聯系不密切 | |
| C. | 化學研究會造成嚴重的環境污染,最終人類將毀滅在化學物質中 | |
| D. | 化學家可以在微觀層面上操縱分子和原子,組裝分子材料、分子器件和分子機器 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2和O2 | B. | HCl和NH3 | C. | H2和Cl2 | D. | CO和O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 某化學小組采用類似制乙酸乙酯的裝置(如圖),以環己醇制備環己烯:
某化學小組采用類似制乙酸乙酯的裝置(如圖),以環己醇制備環己烯:| 密度 (g/cm3) | 熔點 (℃) | 沸點 (℃) | 溶解性 | |
| 環己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 環己烯 | 0.81 | -103 | 83 | 難溶于水 |
 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com