
| A. | Al | B. | Mg | C. | Fe | D. | Na |
 口算與應用題卡系列答案
口算與應用題卡系列答案 名師點睛字詞句段篇系列答案
名師點睛字詞句段篇系列答案科目:高中化學 來源: 題型:解答題
| 實驗步驟 | 預期現象與結論 |
| 步驟1: | 部分固體不溶解 |
| 步驟2: | |
| 步驟3:繼續步驟2中的(2),進行固液分離,用蒸餾水洗滌固體至洗滌液無色.取少量固體于試管中,滴加過量HCl后,靜置,取上層清液,滴加適量H2O2,充分振蕩后滴加KSCN. |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 加入較多NaHSO4的溶液中:Fe3+、Cl-、NO3-、Na+ | |
| B. | 通入大量CO2氣體的溶液中:Na+、Ba2+、Cl-、NO3- | |
| C. | 通入大量NH3的溶液中:Ca2+、Na+、HCO3-、Cl- | |
| D. | 通入大量SO2氣體的溶液中:Na+、SO32-、NH4+、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| A | B | |
| C | D |
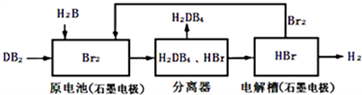
| 化學鍵 | H-H | Br-Br | H-Br |
| 鍵能(kJ/mol) | 436 | 194 | 362 |
| 化學式 | Ag2SO4 | AgBr |
| 溶解度(g) | 0.796 | 8.4×10-6 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
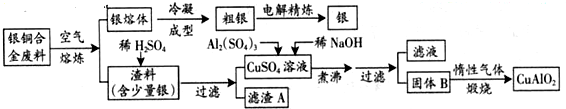
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H+、SO32-、S2-、K+ | B. | Fe3+、Cl-、S2-、Ba2+ | ||
| C. | Cu2+、Cl-、S2-、K+ | D. | Na+、K+、S2-、SO42- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com