
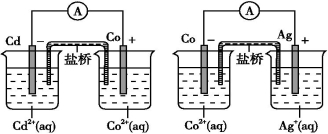
根據如圖,可判斷出下列離子方程式中錯誤的是 ( )
A.2Ag(s)+Cd2+(aq) 2Ag+(aq)+Cd(s) B.Co2+(aq)+Cd(s)
2Ag+(aq)+Cd(s) B.Co2+(aq)+Cd(s) Co(s)+Cd2+(aq)
Co(s)+Cd2+(aq)
C.2Ag+(aq)+Cd(s) 2Ag(s)+Cd2+(aq) D.2Ag+(aq)+Co(s)
2Ag(s)+Cd2+(aq) D.2Ag+(aq)+Co(s) 2Ag(s)+Co2+(aq)
2Ag(s)+Co2+(aq)
A
【解析】
試題分析:金屬活性性:Cd>Co>Ag,所以陽離子氧化性:Ag+> Co2+> Cd2+.由于Cd活動性大于Co,所以Cd失去電子,作還原劑,Co2+得到電子,作氧化劑,所以2Ag(s)+Cd2+(aq)== 2Ag+(aq)+Cd(s)不能發生反應;選項A錯誤;由于氧化性:Co2+> Cd2+;所以Co2+(aq)+Cd(s)== Co(s)+Cd2+(aq) 能發生反應,選項B正確;由于氧化性:Ag+> Cd2+,所以2Ag+(aq)+Cd(s)== 2Ag(s)+Cd2+(aq) ;選項C正確;由于氧化性:Ag+> Co2+,所以2Ag+(aq)+Cd(s)== 2Ag(s)+Cd2+(aq) ;選項D正確。
考點:考查物質的氧化性、還原性的比較及應用的知識。


科目:高中化學 來源:2015屆河北省“五個一名校聯盟”高三教學質量監測(一)化學試卷(解析版) 題型:選擇題
下列說法不正確的是
A.膠體的分散質粒子直徑大小介于溶液與濁液之間
B.金屬冶煉通常利用氧化還原反應原理
C.陶瓷、水泥和光導纖維均屬于硅酸鹽材料
D.“煤改氣”、“煤改電”等清潔燃料改造工程有利于減少霧霾天氣
查看答案和解析>>
科目:高中化學 來源:2015屆江西省高三暑期化學試卷(解析版) 題型:選擇題
在過量的稀硫酸溶液中加入5.6g鐵粉,待反應完全后,再加入50 mL 0.5mol·L-1 KNO3溶液,恰好反應完全。該反應的方程式為:__FeSO4+__KNO3+__H2SO4===__K2SO4+__Fe2(SO4)3+__NxOy +__H2O,則對該反應的下列說法正確的是( )。
A.反應中還原產物是NO
B.化學方程式中按物質順序的計量數是:8、2、5、1、4、1、5
C.反應過程中轉移的電子數為8e-
D.氧化產物和還原產物的物質的量之比為1∶4
查看答案和解析>>
科目:高中化學 來源:2015屆江西省高三上學期第一次月考化學試卷(解析版) 題型:選擇題
將8gFe2O3投入150mL某濃度的稀硫酸中,再投入7g鐵粉收集到1.68LH2(標準狀況),同時,Fe和Fe2O3均無剩余,為了中和過量的硫酸,且使溶液中鐵元素完全沉淀,共消耗4 mol·L-1的NaOH溶液150 mL。則原硫酸的物質的量濃度為 ( )
A.1.5 mol·L-1 B.0.5 mol·L-1 C.2 mol·L-1 D. 1.2 mol·L-1
查看答案和解析>>
科目:高中化學 來源:2015屆江西省高三上學期第一次月考化學試卷(解析版) 題型:選擇題
當向盛有氯化鐵溶液的燒杯中同時加入鐵粉和銅粉,反應結束后,燒杯底部不可能出現的是
A.有銅無鐵 B.有鐵無銅 C.有鐵有銅 D.無鐵無銅
查看答案和解析>>
科目:高中化學 來源:2015屆江西省第一學期高三第一次月考化學(A卷)試卷(解析版) 題型:填空題
有難溶于水的粉末狀固體樣品,可能含Al、Fe2O3、Cu2O、SiO2、Fe3O4中的一種或幾種。研究小組通過實驗確定樣品的成分。
查閱資料知:Cu2O + 2H+ = Cu + Cu2+ + H2O;
部分氫氧化物在溶液中沉淀的pH見下表:
物質 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
開始沉淀的pH | 1.8 | 6.3 | 5.2 |
完全沉淀的pH | 3.0 | 8.3 | 6.7 |
注:金屬離子的起始濃度為0.1 mol·L-1 實驗步驟:
Ⅰ.取一定量樣品于燒杯中,加足量NaOH溶液,有氣體產生,過濾得固體A和無色溶液B;
Ⅱ.向B中加入稀硫酸,出現白色沉淀,繼續滴加稀硫酸至過量,白色沉淀完全溶解;
Ⅲ.向A中加入足量稀硫酸并微熱,固體完全溶解,得溶液C;
Ⅳ.向C中加入NaClO,調節溶液的pH至4~5,產生紅褐色沉淀,過濾得到藍綠色溶液D;
Ⅴ.向D中加入NaOH,調節溶液的pH到7~8,產生藍色絮狀沉淀。
請回答下列問題。
(1)Ⅰ中產生氣體的離子方程式為 。
(2)由Ⅰ、Ⅱ知,原樣品中一定不存在的物質是 。
(3)溶液C中除H+、Cu2+外一定還含有另一種陽離子;為驗證溶液C中存在該陽離子,可選用的試劑及對應的現象是 。
(4)Ⅳ中加NaClO的目的是 。
(5)將Ⅳ中得到的溶液D電解,若電路中有0.1mol電子通過,則理論上陰極質量增重 g。
(6)由上述實驗可以獲得結論:原樣品所有可能的成分組合為組合1: ;組合2:
;……(用化學式表示)
查看答案和解析>>
科目:高中化學 來源:2015屆江西省第一學期高三第一次月考化學(A卷)試卷(解析版) 題型:選擇題
下列研究目的和示意圖相符的是( )
| A | B | C | D |
研 究 目 的 | 固定容積的密閉容器中,壓強對反應: 2SO2(g)+O2(g) | 固定容積的密閉容器中,溫度對反應: N2(g) +3H2(g) | 固定容積的密閉容器中,增大CO2濃度,對已達平衡的反應: CO(g)+H2O(g) | 等質量Na、K 分別與足量水反應 |
示 意 圖 |
|
|
|
|
查看答案和解析>>
科目:高中化學 來源:2015屆江西省高三上學期第一次月考化學試卷(解析版) 題型:填空題
氨在國民經濟中占有重要地位。
(1)NH3的電子式為
(2)實驗室中制取氨氣的化學方程式為 ,
(3)欲快速制取氨氣,可將濃氨水滴入固體氫氧化鈉中,其裝置如下圖,請結合化學用語 從化學平衡的角度解釋:
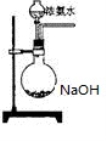
(4)將SO2氣體通入氯化鋇溶液,未見有沉淀生成,繼續通入NH3,則出現白色沉淀,請寫出反應的離子方程式 ;若將SO2氣體通入酸化的硝酸鋇溶液,也產生白色沉淀,用離子方程式加以說明
(5)氨和肼(N2H4)是氮的兩種常見化合物,在科學技術和生產中有重要的應用。
肼——空氣燃料電池是一種堿性電池,該電池放電時,負極的反應式 。
(6)氮氧化物的排放會對空氣造成污染,利用氧化法除去煙氣中的氮氧化物。
首先向氮氧化物中補充氧氣,然后將混合氣體通入石灰乳中,使之轉化為硝酸鈣。
已知某氮氧化物由NO和NO2組成,且n(NO):n(NO2)=1:3.
寫出氧化吸收法除去氮氧化物的化學方程式______________ _____
查看答案和解析>>
科目:高中化學 來源:2015屆江西省南昌市三校高三上第一次聯考化學試卷(解析版) 題型:實驗題
(14分)為了證明在實驗室制備Cl2的過程中會有水蒸氣和HCl揮發出來,甲同學設計了如下圖所示的實驗裝置,按要求回答問題。
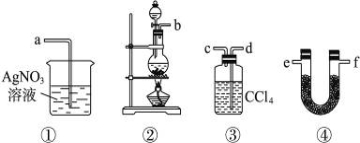
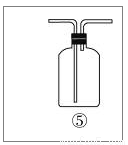
(1)請根據甲同學的意圖,連接相應的裝置,接口的順序:b接___,___接___,___接a
(2)U形管中所盛試劑的化學式為_________________。
(3)裝置③中CCl4的作用是________________。
(4)乙同學認為甲同學實驗有缺陷,不能證明最終通入AgNO3溶液中的氣體只有一種。為了確保實驗結論的可靠性,證明最終通入AgNO3溶液的氣體只有一種,乙同學提出在某兩個裝置之間再加裝置⑤。你認為裝置⑤應加在 之間(填裝置序號)。瓶中可以放入__________________。
(5)丙同學看到甲同學設計的裝置后提出無需多加裝置,只需將原來燒杯中AgNO3溶液
換成其它溶液。你認為可將溶液換成_____________,如果觀察到____________
_________的現象,則證明制Cl2時有HCl揮發出來。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com