
| 溫度/K | 反應I | 反應II | 已知: K1>K2>K1′>K2′ |
| 298 | K1 | K2 | |
| 328 | K1′ | K2′ |
分析 (1)根據反應中氣體的體積減小可判斷反應的焓變減小,平衡常數等于生成物的平衡濃度冪之積除以反應物的平衡濃度冪之積,從圖中數據可知溫度升高反應Ⅰ和Ⅱ的平衡常數均減小,所以反應Ⅰ和Ⅱ均是放熱反應,△H1、△H2小于0,利用蓋斯定律Ⅰ×2+Ⅱ得反應Ⅲ,根據△H1、△H2判斷△H3的正負,確定反應Ⅲ的熱效應;
(2)依據化學平衡移動的原理:減小生成物濃度平衡向正方向移動,增大反應物濃度平衡向正方向移動;
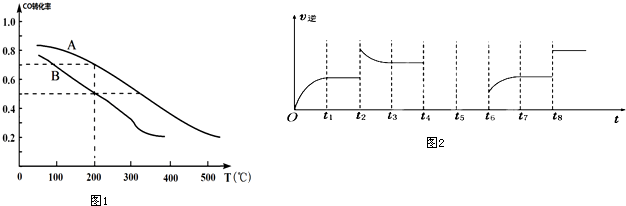
(3)增大壓強,平衡向正反應方向移動,結合圖象,判斷A、B兩條曲線對應的壓強,從方程式可知,反應物有3mol氣體,生成物有2mol氣體,所以壓強增大時平衡氣體體積減小的方向移動,即正向移動,在200℃時,轉化率高的壓強大,故A曲線對應壓強為5.0MPa,曲線對應壓強為0.1MPa,從圖中可知壓強為0.1MPa、溫度為200℃時CO的轉化率為0.5,然后利用三段式列式計算甲醇物質的量分數=$\frac{甲醇物質的量}{平衡混合氣體總物質的量}$×100%;
(4)①該反應是一個反應前后氣體體積減小的且正反應是放熱的化學反應,t2時逆反應速率增大,且平衡時反應速率大于t2時反應速率,平衡向逆反應方向移動;
②t4時降壓,逆反應速率減小,平衡逆向移動,隨著反應的進行,逆反應速率減小,在t5時達到新的平衡狀態,t6時增大反應物的濃度,t6點逆反應速率不變,平衡向正反應方向移動,隨著反應的進行,逆反應速率增大,大于原平衡濃度,據此畫出變化的圖象.
解答 解:(1)CO(g)+2H2(g)?CH3OH(g)是一個氣體體積減小的反應,所以熵值減小,△S<0,
依據方程式2CH3OH(g)?CH3OCH3(g)+H2O(g)可知平衡常數K=$\frac{[C{H}_{3}OC{H}_{3}][{H}_{2}O]}{[C{H}_{3}OH]}$,
從圖中數據可知溫度升高反應Ⅰ和Ⅱ的平衡常數均減小,所以反應Ⅰ和Ⅱ均是放熱反應,△H1、△H2都小于0,利用蓋斯定律Ⅰ×2+Ⅱ得反應Ⅲ,則△H3=2×△H1+△H2,△H1、△H2都小于0,所以△H3=2×△H1+△H2<0,故反應Ⅲ是放熱反應,
故答案為:<;$\frac{[C{H}_{3}OC{H}_{3}][{H}_{2}O]}{[C{H}_{3}OH]}$;放熱;
(2)依據化學平衡移動原理:減小生成物濃度平衡向正方向移動,增大反應物濃度平衡向正方向移動,在CO(g)+H2O(g)?CO2(g)+H2(g)中反應消耗了H2O(g)有利于反應II、III正向移動;同時此反應生成了H2,有利于反應I、III正向移動,
故答案為:此反應消耗了H2O(g)有利于反應II、III正向移動;同時此反應生成了H2,有利于反應I、III正向移動;
(3)從方程式可知,反應物有3mol氣體,生成物有2mol氣體,所以壓強增大時平衡氣體體積減小的方向移動,即正向移動,在200℃時,轉化率高的壓強大,故A曲線對應壓強為5.0MPa,曲線對應壓強為0.1MPa,從圖中可知壓強為0.1MPa、溫度為200℃時CO的轉化率為0.5,
設加入COamol,則有H22amol
CO(g)+2H2(g)?CH3OH(g).
反應前(mol) a 2a 0
反應了(mol) 0.5a a 0.5a
平衡時(mol) 0.5a a 0.5a
可求得$\frac{0.5a}{0.5a+a+0.5a}$×100%=25%
故答案為:25%;
(4)①該反應是一個反應前后氣體體積減小的且是正反應是放熱的化學反應,t2時逆反應速率增大,且平衡時反應速率大于t2時反應速率,平衡向逆反應方向移動,改變的條件為增大生成物C濃度或升高溫度;
故答案為:增大生成物C濃度;升高溫度;
②t4時降壓,逆反應速率減小,平衡逆向移動,隨著反應的進行,逆反應速率減小,在t5時達到新的平衡狀態,t6時增大反應物的濃度,t6點逆反應速率不變,平衡向正反應方向移動,隨著反應的進行,逆反應速率增大,大于原平衡濃度,所以其圖象為: ,
,
故答案為: .
.
點評 本題考查了熵變焓變的判斷、化學平衡常數表達式的書寫、外界條件對反應速率的影響等知識點,看清圖象表達的含義是解題的關鍵所以,圖象的理解和繪制是解題難點,題目難度中等.


科目:高中化學 來源: 題型:解答題
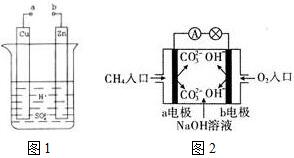 原電池是化學對人類的一項重大貢獻.
原電池是化學對人類的一項重大貢獻.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 其他條件不變,減小容器體積,平衡不移動 | |
| B. | 其他條件不變,增大c(A),A的轉化率增大 | |
| C. | 降低溫度,v正增大,v逆減小 | |
| D. | v正(A)═2v逆(C) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 同素異形體:是否由同一種原子構成 | |
| B. | 純凈物和混合物:是否只含一種元素 | |
| C. | 電解質和非電解質:溶于水或熔融狀態下能否導電 | |
| D. | 氧化還原反應:元素化合價是否變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亞硫酸 |
| 電離平衡常數 (25℃) | Ka=1.75ⅹ10-5 | Ka=2.98ⅹ10-8 | Ka1=4.3ⅹ10-7 Ka2=5.61ⅹ10-11 | Ka1=1.54ⅹ10-2 Ka2=1.02ⅹ10-7 |
| A. | 少量的CO2通入NaClO溶液中:CO2+H2O+2ClO-═CO32-+2HClO | |
| B. | 少量的SO2通入Na2CO3溶液中:SO2+H2O+2CO32-═SO32-+2HCO3- | |
| C. | 少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| D. | 相同濃度的NaHCO3溶液與NaHSO3溶液等體積混合:H++HCO3-═CO2↑+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | O2和O3的混合物共16g,其中所含氧原子數為NA | |
| B. | 1.0L 0.1mol/L的AlCl3溶液中含有的鋁離子數為0.1NA | |
| C. | 28g乙烯中所含有共用電子對數目為4NA | |
| D. | 1mol金屬鈉完全轉化為Na2O2所轉移的電子數目為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 | |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |


查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 穩定性:PH3>H2S>HCl | B. | 酸性:HClO4>HBrO4>HIO4 | ||
| C. | 非金屬性:F>O>S | D. | 堿性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com