
| ||
| 高溫高壓 |
| ||
| 高溫高壓 |
| ||
| 高溫高壓 |
| 50 |
| 3 |
| 100 |
| 3 |
| 100/3×22.4L |
| 20.0×103L |
| 2×98 |
| 10.0t×98% |
| 2×136+234 |
| x |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
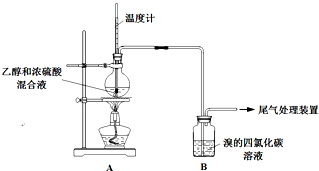 實驗室制乙烯時,產生的氣體能使Br2 的四氯化碳溶液褪色,甲、乙同學用如圖實驗驗證.(氣密性已檢驗,部分夾持裝置略).
實驗室制乙烯時,產生的氣體能使Br2 的四氯化碳溶液褪色,甲、乙同學用如圖實驗驗證.(氣密性已檢驗,部分夾持裝置略).| 操 作 | 現 象 |
| 點燃酒精燈, 加熱至170℃ | Ⅰ:A中燒瓶內液體漸漸變黑 Ⅱ:B內氣泡連續冒出,溶液逐漸褪色 |
| … | |
| 實驗完畢, 清洗燒瓶 | Ⅲ:A中燒瓶內附著少量黑色顆粒狀物,有刺激性氣味逸出 |
| 設 計 | 現 象 | |
| 甲 | 在A、B間增加一個裝有某種試劑的洗氣瓶 | Br2的CCl4溶液褪色 |
乙 | 與A連接的裝置如下: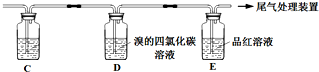 | D中溶液由紅棕色變為淺紅棕色時,E中溶液褪色 |
查看答案和解析>>
科目:高中化學 來源: 題型:
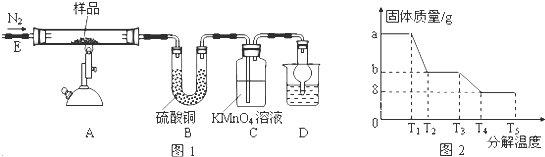
查看答案和解析>>
科目:高中化學 來源: 題型:
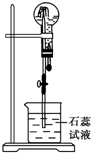 物質A是一種白色晶體,它與濃NaOH溶液共熱,放出無色氣體B,用圓底燒瓶收集干燥的B.按如圖所示裝置儀器,擠壓滴管的膠頭時,可以得到藍色噴泉;A與濃硫酸反應,放出無色氣體C,用圓底燒瓶收集干燥的C,仍按如圖所示裝置儀器,擠壓滴管的膠頭時,可以得到紅色噴泉.
物質A是一種白色晶體,它與濃NaOH溶液共熱,放出無色氣體B,用圓底燒瓶收集干燥的B.按如圖所示裝置儀器,擠壓滴管的膠頭時,可以得到藍色噴泉;A與濃硫酸反應,放出無色氣體C,用圓底燒瓶收集干燥的C,仍按如圖所示裝置儀器,擠壓滴管的膠頭時,可以得到紅色噴泉.查看答案和解析>>
科目:高中化學 來源: 題型:

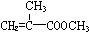 ) 合成路線的一部分.現在人們利用最新開發的+2價鈀的均相鈀催化劑體系,將丙炔在甲醇和一氧化碳存在下,于60℃、6MPa條件下羰基化,一步制得
) 合成路線的一部分.現在人們利用最新開發的+2價鈀的均相鈀催化劑體系,將丙炔在甲醇和一氧化碳存在下,于60℃、6MPa條件下羰基化,一步制得 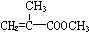 ,其化學方程式為:
,其化學方程式為: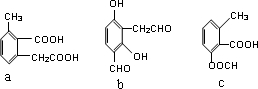 .
.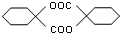 ,模仿以上流程圖設計合成路線,標明每一步的反應物及反應條件.(有機物寫結構簡式,其它原料自選)
,模仿以上流程圖設計合成路線,標明每一步的反應物及反應條件.(有機物寫結構簡式,其它原料自選)| 濃硫酸 |
| 170℃ |
| 高溫、高壓 |
| 催化劑 |
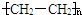 .
.查看答案和解析>>
科目:高中化學 來源: 題型:
| A、用NaCl固體和濃硫酸各自配制0.5mol.L-1的溶液,所用儀器完全相同 |
| B、酸式滴定管注入NaHCO3溶液之前應進行撿漏、洗滌和潤洗 |
| C、過濾、溶解、蒸發操作中都需要使用玻璃棒 |
| D、用小試管和膠頭滴管不能鑒別出Na2CO3溶液、稀鹽酸、Ba(OH)2溶液、酚酞試液 |
查看答案和解析>>
科目:高中化學 來源: 題型:
A、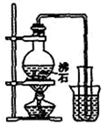 制取少量蒸餾水 |
B、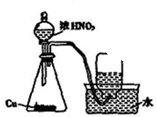 用銅和濃硝酸制取少量NO3 |
C、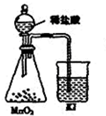 比較MnO2、Cl2、I2的氧化性 |
D、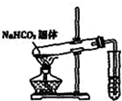 探究NaHCO3的熱穩定性 |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
| A、常溫下,氨水與(NH4)2SO4溶液混合后pH=7的溶液中,c(NH4+):c(SO42-) |
| B、相同溫度下,1 mol.L-1醋酸與0.5mol.L-1醋酸中c(H+)之比 |
| C、用同濃度鹽酸中和相同體積pH均為12的Ba(OH)2和KOH,所需鹽酸的體積之比 |
| D、pH=2的H2SO4溶液與pH=2的CH3COOH溶液中,c(CH3COOH):c(H2SO4) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com