
| A、常溫下,氨水與(NH4)2SO4溶液混合后pH=7的溶液中,c(NH4+):c(SO42-) |
| B、相同溫度下,1 mol.L-1醋酸與0.5mol.L-1醋酸中c(H+)之比 |
| C、用同濃度鹽酸中和相同體積pH均為12的Ba(OH)2和KOH,所需鹽酸的體積之比 |
| D、pH=2的H2SO4溶液與pH=2的CH3COOH溶液中,c(CH3COOH):c(H2SO4) |


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| 丁 |
| 丁 |
| 甲 |
| A、若甲為焦炭,則丁可能是O2 |
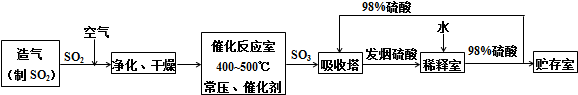
| B、若甲為SO2,則丁可能是氨水 |
| C、若甲為NaAlO2溶液,則丁可能是鹽酸 |
| D、若甲為CuCl2,則丁可能是氨水. |
查看答案和解析>>
科目:高中化學 來源: 題型:
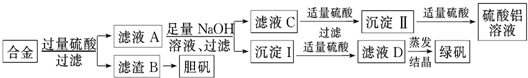
| A、x等于6 |
| B、性質穩定,不易脫色 |
| C、易溶于強酸和強堿 |
| D、可用氧化物形式表示BaO?CuO?2SiO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
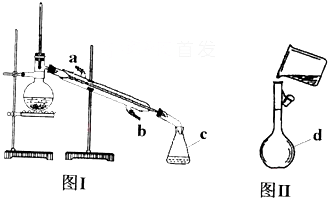
| A、分液操作時,分液漏斗中下層液體從下口放出,上層液體從上口倒出 |
| B、蒸餾操作時,應使溫度計水銀球靠近蒸餾燒瓶的底部 |
| C、萃取操作時,應選擇有機萃取劑,且萃取劑的密度必須必水大 |
| D、蒸發操作時,應使混合物中的水分完全蒸干后,才能停止加熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| 化學式 | 電離常數 |
| HClO | Ka=3×10-8 |
| H2CO3 | Ka1=4.3×10-7 |
| Ka2=5.6×10-11 | |
| CH3COOH | Ka=1.8×10-5 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、已知稀鹽酸和稀NaOH溶液反應生成1molH2O時放出57.3kJ的熱量,則稀硫酸和氫氧化鋇溶液反應生成1molH2O時也放出57.3kJ的熱量 | ||
B、C(石墨)+
| ||
| C、同溫同壓下,H2(g)+Cl2(g)=2HCl(g)在光照和點燃條件下的△H不同 | ||
| D、已知:①S(g)+O2(g)=SO2(g)△H=akJ.mol-1②S(s)+O2(g)=SO2(g)△H=bkJ.mol-1,則a<b |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com