
| A. | 兩種不同的元素不可能既在同一周期,又在同一主族 | |
| B. | 元素周期表中的元素不全是從自然界中發現的 | |
| C. | 周期表中共1-20號元素,含有非金屬11種 | |
| D. | 若周期表中第8周期完全填滿,此周期應含有有50種元素 |
分析 A、元素種類不同,質子不同,所以在元素周期表中應在不同的位置;
B、周期表中的元素大多是自然界存在的,但有些屬于人造元素,如106號元素;
C、H、He、B、C、N、O、F、Ne、Si、P、S、Cl、Ar,13種非金屬元素;
D、因為第八能層有s.p.d.f.g能級,其中S能級一軌道,能容納2電子,p能級三軌道,能容納六電子(第一周期只有s,第二三周期s.p),d能級五軌道,能容納十電子(四五周期),f能級七軌道,能容納十四個(六七周期),第八周期將出現g能級,九軌道十八電子,所以能容納50種.
解答 解:A、元素種類不同,質子不同,所以在元素周期表中應在不同的位置,所以兩種不同的元素不可能既在同一周期,又在同一主族,故A正確;
B、周期表中的元素大多是自然界存在的,但有些屬于人造元素,都是放射性元素,包括Tc、Pm、At、Np、Pu、Am、Cm、Bk、Cf、Es、Fm、Md、No、Lr、Rf、Db、Es、Bh、Hs、Mt和110、111、112號元素,故B正確;
C、H、He、B、C、N、O、F、Ne、Si、P、S、Cl、Ar,13種非金屬元素,而不是11種,故C錯誤;
D、因為第八能層有s.p.d.f.g能級,其中S能級一軌道,能容納2電子,p能級三軌道,能容納六電子(第一周期只有s,第二三周期s.p),d能級五軌道,能容納十電子(四五周期),f能級七軌道,能容納十四個(六七周期),第八周期將出現g能級,九軌道十八電子,所以能容納50種,故D正確;
故選C.
點評 本題考查元素周期表的結構及應用,為高頻考點,把握周期表中族和周期的劃分及元素的位置為解答的關鍵,題目難度不大.


 口算題卡北京婦女兒童出版社系列答案
口算題卡北京婦女兒童出版社系列答案科目:高中化學 來源: 題型:多選題
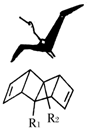 始祖鳥烯形狀宛如一只展翅飛翔的鳥,其鍵線式結構表示如圖,其中R1、R2為烷烴基.則下列有關始祖鳥烯的說法中正確的是( )
始祖鳥烯形狀宛如一只展翅飛翔的鳥,其鍵線式結構表示如圖,其中R1、R2為烷烴基.則下列有關始祖鳥烯的說法中正確的是( )| A. | 始祖鳥烯與乙烯互為同系物 | |
| B. | 若R1=R2=甲基,則其化學式C12H14 | |
| C. | 若R1=R2=甲基,則始祖鳥烯的一氯代物有3種 | |
| D. | 始祖鳥烯既能使酸性高錳酸鉀褪色,也能使溴水褪色,則兩反應的反應類型是相同的 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2O與D2O互稱同素異形體 | |
| B. | 1H與D互稱同位素 | |
| C. | 氘(D)原子核外有1個電子 | |
| D. | 1H218O與D216O的相對分子質量相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含0.1 mol BaCl2的溶液中Cl-數為0.1NA | |
| B. | 1molCl2與足量Fe反應,轉移的電子數為3NA | |
| C. | 11.2 L CO2所含有的分子數為0.5NA | |
| D. | 標準狀況下,分子數為NA的CO、N2混合氣體體積約為22.4 L,質量為28 g |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 苯中的甲苯(溴水、分液) | B. | 乙醇中的乙酸(NaOH溶液,分液) | ||
| C. | 乙醇中的水(新制CaO,蒸餾) | D. | 乙酸乙酯中的乙酸(NaOH溶液,分液) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 醋酸溶液與水垢中的CaCO3反應:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | NH4HCO3溶于過量的NaOH溶液中:HCO3-+OH-═CO32-+H2O | |
| C. | 將氯氣溶于水制備次氯酸:Cl2+H2O═2H++Cl-+ClO- | |
| D. | Fe3O4溶于足量濃鹽酸:Fe3O4+8H+═Fe2++2Fe3++4H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4.6g 金屬鈉與足量乙醇反應放出2.24L氫氣 | |
| B. | 50mL 18.4 mol/L濃硫酸與足量銅加熱反應,生成SO2分子的數目為0.46NA | |
| C. | 1mol羥基(-OH)中含電子數為10NA | |
| D. | 常溫下,10L pH=12的Na2CO3溶液中含有的OH-離子數目為0.1NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com