
【題目】[化學―有機化學基礎]
化合物M是二苯乙炔類液晶材料的一種,最簡單的二苯乙炔類化合物是![]() 。以互為同系物的單取代芳香烴A、G為原料合成M的一種路線(部分反應條件略去)如下:
。以互為同系物的單取代芳香烴A、G為原料合成M的一種路線(部分反應條件略去)如下:
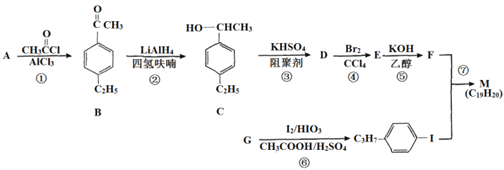
回答下列問題:
⑴G的結構簡式為_____________________
⑵C中含有的官能團名稱是________
⑶反應②的反應類型是_________,反應⑥的反應類型是______
⑷反應⑤的化學方程式為________________________
⑸能同時滿足下列條件的B的同分異構體有____種(不考慮立體異構),其中核磁共振氫譜為5組峰,且峰面積之比為6:2:2:l:l的是_________(寫結構簡式)。
①苯環上有兩個取代基 ②能發生銀鏡反應
⑹參照上述合成路線,設計一條由苯乙烯和甲苯為起始原料制備![]() 的合成路線_________。
的合成路線_________。
【答案】 ![]() 羥基 還原反應 取代反應
羥基 還原反應 取代反應 ![]() +2KOH
+2KOH![]()
![]() +2KBr+2H2O 15
+2KBr+2H2O 15 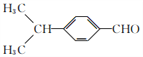
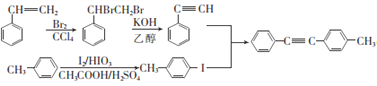
【解析】試題分析:本題考查有機推斷和有機合成,有機物結構簡式和有機方程式的書寫,官能團的識別,有機反應類型的判斷,限定條件同分異構體數目的確定和書寫,有機合成路線的設計。A是單取代芳香烴,根據反應①和B的結構簡式可逆推出A的結構簡式為![]() ;A、G互為同系物,G是單取代芳香烴,根據反應⑥及其生成物的結構簡式可逆推出G的結構簡式為
;A、G互為同系物,G是單取代芳香烴,根據反應⑥及其生成物的結構簡式可逆推出G的結構簡式為![]() ;C發生反應③生成D,D與Br2/CCl4發生加成反應生成E,E與KOH/乙醇作用發生消去反應生成F,結合C的結構簡式,D的結構簡式為
;C發生反應③生成D,D與Br2/CCl4發生加成反應生成E,E與KOH/乙醇作用發生消去反應生成F,結合C的結構簡式,D的結構簡式為![]() ,E的結構簡式為
,E的結構簡式為![]() ,F的結構簡式為
,F的結構簡式為![]() 。化合物M是二苯乙炔類液晶材料的一種,結合M的分子式C19H20,反應⑦為取代反應,M的結構簡式為
。化合物M是二苯乙炔類液晶材料的一種,結合M的分子式C19H20,反應⑦為取代反應,M的結構簡式為![]() 。
。
(1)G的結構簡式為![]() 。
。
(2)根據C的結構簡式知,C中含有的官能團的名稱是羥基。
(3)對比B和C的結構簡式,B→C為羰基還原為羥基,反應②為還原反應。反應⑥為G中—C3H7對位的苯環氫原子被I取代,反應⑥為取代反應。
(4)反應⑤為E發生消去反應生成F,化學方程式為![]() +2KOH
+2KOH![]()
![]() +2KBr+2H2O。
+2KBr+2H2O。
(5)B的同分異構體能發生銀鏡反應,B的同分異構體中含醛基,B的同分異構體的苯環上有兩個取代基,兩個取代基可以為:①—CHO和—CH2CH2CH3,②—CHO和—CH(CH3)2,③—CH2CHO和—CH2CH3,④—CH2CH2CHO和—CH3,⑤![]() 和—CH3,當苯環上有兩個取代基時,兩個取代基有鄰、間、對三種位置,則滿足條件的B的同分異構體有5
和—CH3,當苯環上有兩個取代基時,兩個取代基有鄰、間、對三種位置,則滿足條件的B的同分異構體有5![]() 3=15種。其中核磁共振氫譜為5組峰,且峰面積之比為6:2:2:1:1的同分異構體的結構簡式為
3=15種。其中核磁共振氫譜為5組峰,且峰面積之比為6:2:2:1:1的同分異構體的結構簡式為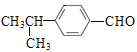 。
。
(6)對比![]() 、
、![]() 和
和![]() 結構簡式,聯想流程中反應⑦,由
結構簡式,聯想流程中反應⑦,由![]() 合成
合成![]() ,由
,由![]() 合成
合成![]() ;
;![]() 合成
合成![]() 模仿流程中反應④、反應⑤,
模仿流程中反應④、反應⑤,![]() 合成
合成![]() 模仿流程中反應⑥;合成路線的流程圖為:
模仿流程中反應⑥;合成路線的流程圖為:
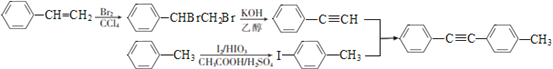 。
。


 云南師大附小一線名師提優作業系列答案
云南師大附小一線名師提優作業系列答案 沖刺100分單元優化練考卷系列答案
沖刺100分單元優化練考卷系列答案科目:高中化學 來源: 題型:
【題目】下列化學用語正確的是
A. 丙烯的電子式為: ![]()
B. 二乙酸乙二酯的結構簡式為: ![]()
C. 苯酚鈉溶液中通入少量CO2的離子方程式為:![]() +H2O+CO2
+H2O+CO2![]()
![]() +HCO3—
+HCO3—
D. 甲醛與足量的銀氨溶液反應的化學方程式為:HCHO+2Ag(NH3)2OH ![]() HCOONH4+2Ag↓+3NH3+H2O
HCOONH4+2Ag↓+3NH3+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以鉻鐵礦[主要成分為Fe(CrO2)2;還含有Al2O3、Fe2O3、SiO2等雜質]為主要原料生產重鉻酸鈉晶體(Na2Cr2O7·2H2O,Na2Cr2O7是一種強氧化劑)的主要工藝流程如下:
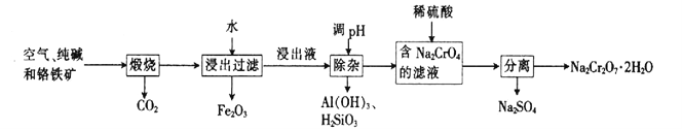
(1)亞鉻酸亞鐵[Fe(CrO2)2]中Cr的化合價是___________。
(2)煅燒生成Na2CrO4的化學方程式為___________。
(3)酸化濾液Na2CrO4時,不選用赴酸的原因是____________________,從平衡角度分析酸化的原理:______________________。
(4)該工藝中某種產物可以再利用,該物質的化學式為________________。
(5)采用石墨電極電解Na2CrO4溶液,可實現Na2CrO4→Na2Cr2O7的轉化,其原理如圖所示。,
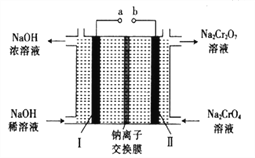
①寫出Ⅰ電極的電極反應式_______________________。
②當Na2CrO4轉化為1malNa2Cr2O7時,理輪上Ⅱ電極上轉移電子的物質的量為________。
(3)稱取2.500g重鉻酸鈉晶體試樣,加入蒸餾水配制成250ml溶液,從中取出25.00mL于碘量瓶中,向其中加入10mL2mol·L-1 H2SO4溶液和足量碘化鉀(鉻的還原產物為Cr3+),放于暗處5min。然后加入100mL水,加入3mL淀粉指示劑,用0.120mol·L-1的Na2S2O3標準溶液進行滴定(發生反應:I2+2S2O32-=2I-+S4O62-)。
①判斷達到滴定終點的依據是______________________。
②若實驗中共用去40.00mL,Na2S2O3標準溶液。則所得產品的純度為_____________(設整個過程中其他雜質不參如反應)(保留3位有效數字)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關離子方程式或離子共存的敘述正確的是
A. 將磁性氧化鐵溶于氫碘酸: Fe3O4+ 8H+= 2Fe3++ Fe2+ + 4H2O
B. 用肥皂(主要成份C17H35COONa)檢驗含有較多鈣離子的硬水:2C17H35COO-+Ca2+=(C17H35COO)2Ca↓
C. 常溫下,在![]() =0.1的溶液中:Na+、K+、AlO2-、HCO3-能大量共存
=0.1的溶液中:Na+、K+、AlO2-、HCO3-能大量共存
D. 在NaClO溶液中:SO32-、OH-、Cl-、K+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】草酸晶體(H2C2O4·2H2O)無色,熔點為101℃,易溶于水,受熱脫水、升華,170℃以上分解。某學生擬用下圖裝置做草酸晶體的分解實驗并驗證部分產物,下列說法錯誤的是
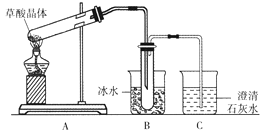
A. 裝置A中的大試管口應略向下傾斜,是因為加熱草酸晶體時會產生水
B. 裝置B的主要作用是冷凝(水蒸氣、草酸)等,防止草酸進入裝置C中,干擾CO2的檢驗
C. 裝置C中可觀察到的現象是有氣泡冒出,澄清石灰水變渾濁
D. 本實驗能證明草酸晶體的分解產物有二氧化碳
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據元素周期表和元素周期律,判斷下列敘述不正確的是

A. 氣態氫化物的穩定性:H2O>NH3>SiH4
B. 氫元素與其他元素可形成共價化合物或離子化合物
C. 上圖所示實驗可證明元素的非金屬性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118號元素在周期表中位于第七周期0族
”(ào)命名的第118號元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H、C、N、O、F、Ca是六種重要的元素請根據所學的物質結構與性質的4機關知識下列問題:
(1)基態碳原子的電子排布式為__,O和F形成的化合物中原子價層都滿足8電子結構的結構式是__,O元素的化合價為________.
(2)Ca在燃燒時產生紅色火焰,其焰色反應看見的光屬于__(填“吸收”或“發射”)光譜。
(3)某藥物的結構簡式為![]() ,財該物質中氮原子的雜化軌道類型為____,其分子之間__(填“能”或“不能”)形成氫鍵。
,財該物質中氮原子的雜化軌道類型為____,其分子之間__(填“能”或“不能”)形成氫鍵。
(4)CO2屬于_____(填“極性”或”非極性”)分子。CO32-的空間構型為_____,與其互為等電子體的分子和離子分別為_________(各寫一種)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知化合物C為中學常見的化合物。
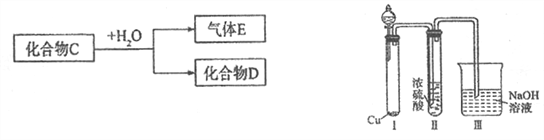
(1)若D是一種強酸,則C與水反應的化學方程式為__________________________。
有人認為“濃H2SO4可以干燥氣體C”,某同學為了驗證該觀點是否正確,用如右上圖裝置進行實驗。分液漏斗中應加入_______________,打開分液漏斗進行實驗,過程中,濃H2SO4中未發現有氣體逸出,且變為紅棕色,則你得出的解釋和結論是__________________。
(2)若D是一種常見的強堿,則C的電子式為:_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】
(1)上圖四個裝置常用于實驗室制取氣體,其中制取氯氣選用的裝置為_______________,反應的離子方程式為______________________。
(2)從下圖裝置左端分別通入氯氣或二氧化硫時,裝置B中觀察到的現象是否相同________(填“相同”或“不相同”);裝置A反應后溶液均褪色,如何利用褪色后的溶液判斷是何種氣體使其褪色______________(寫出簡要的實驗步驟);

(3)裝置F中盛放的溶液為______________(填溶質的化學式);若裝置E中試劑為鐵絲,則通入氯氣與鐵絲充分反應的化學方程式為______________;
(4)當通入足量SO2完全反應后,向C中滴加淀粉溶液,無明顯現象。該反應的離子方程式為______________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com