

分析 (1)①先判斷金屬離子的化合價,再根據根據核外電子排布式的書寫規則書寫,注意3d能級的能量大于4s能級的能量,失電子時,先失去最外層上的電子;N、O、S三種元素中由于N原子的2p軌道是半充滿狀態,所以第一電離能最大;同主族元素,隨電子層數的增多,第一電離能逐漸減小;
②根據SO42-中S原子的價層電子對數判斷;原子數相同、價電子數也相同的微粒互為等電子體;
(2)根據相似相容原理判斷;陰陽離子存在離子鍵,非金屬元素間易形成共價鍵,配合物中存在配位鍵;
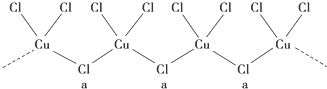
(3)a位置上Cl原子成2個單鍵,含有2對孤對電子,雜化軌道數為4,據此判斷;一種化合物的化學式為KCuCl3,其中銅元素為+2價,故另一種化合物中銅為+1價,CuCl3原子團的化合價為-2,據此書寫;
(4)銅的晶胞為面心立方最密堆積,根據其晶胞的堆積類型判斷,三個銅原子相切,形成晶胞的面對角線,由此得到銅原子半徑;根據銅摩爾質量=摩爾體積×密度計算.
解答 解:(1)①銅是29號元素,根據能量最低原理其態原子的電子排布式為1s22s22p63s23p63d104s1或[Ar]3d104s1,該原子失去一個電子時,生成亞銅離子,失去的電子是最外層電子,所以亞銅離子的基態的電子排布式為:1S22S22P63S23P63d10. 元素周期律中,同一周期元素的第一電離能隨著原子序數的增大而增大,但第ⅡA和第ⅢA、第ⅤA和第ⅥA互換,同一主族元素的第一電離能隨著原子序數的增大而減小,所以其第一電離能大小為N>O>S,
故答案為:1S22S22P63S23P63d10;N>O>S;
②SO42-的價層電子對數=4+$\frac{1}{2}$(6+2-4×2)=4,沒有孤電子對,所以空間構型為正四面體型;與SO42-互為等電子體的有機分子的化學式為是CCl4;
故答案為:正四面體形,CCl4;
(2)在水中得到深藍色透明溶液,加入乙醇析出晶體,說明在乙醇中溶解性降低,根據相似相溶分析:乙醇分子比水分子極性弱,加入乙醇降低溶劑的極性,從而減小溶質的溶解度;[Cu(NH3)4]SO4中硫酸根離子和[Cu(NH3)4]2+存在離子鍵,N原子和銅原子之間存在配位鍵,NH3中H和N之間存在共價鍵,所以[Cu(NH3)4]SO4中所含的化學鍵有共價鍵、離子鍵、配位鍵;
故答案為:乙醇分子比水分子極性弱,加入乙醇降低溶劑的極性,從而減小溶質的溶解度;共價鍵、離子鍵、配位鍵;
(3)a位置上Cl原子成2個單鍵,含有2對孤對電子,雜化軌道數為4,雜化軌道類型為:sp3,一種化合物的化學式為KCuCl3,其中銅元素為+2價,故另一種化合物中銅為+1價,CuCl3原子團的化合價為-2,其化學式為:K2CuCl3,
故答案為:sp3、K2CuCl3;
(4)銅的晶胞為面心立方最密堆積,一個晶胞能分攤到4個Cu原子;晶胞面對角線長為銅原子半徑的四倍,銅原子半徑=$\frac{361×\sqrt{2}}{4}$=128;
1pm=10-10cm,故一個晶胞的體積為(361×10-10)3cm3;
晶胞的質量=體積×密度,一個晶胞的質量為(361×10-10)3cm3×9.00g•cm-3;
在一個體心晶胞含4個銅原子,故銅的摩爾質量=$\frac{1}{4}$×晶胞的質量×NA,
64g•mol-1=$\frac{1}{4}$×(361×10-10)3cm3×9.00g•cm-3×NA,
得NA=$\frac{4×64}{9×(3.61×1{0}^{-8})^{3}}$mol-1,
故答案為:128;$\frac{4×64}{9×(3.61×1{0}^{-8})^{3}}$mol-1.
點評 本題考查了物質結構與性質,題目涉及電子排布式、第一電離能、等電子體、化學鍵、晶胞的計算等,題目難度中等,側重于考查學生對基礎知識的綜合應用能力.


 互動英語系列答案
互動英語系列答案科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com