


 .
. 、
、 .
. 分析 M和氫氧化鈉的水溶液發生水解反應生成A、B和 ,B和硝酸酸化的硝酸銀溶液反應生成淡黃色沉淀AgBr,則B為NaBr,同時說明M中X元素為Br元素,A能連續被氧化,說明A為醇,生成的D為酸,酸能和銀氨溶液發生銀鏡反應,說明D為HCOOH,則A為CH3OH、C為HCHO;
,B和硝酸酸化的硝酸銀溶液反應生成淡黃色沉淀AgBr,則B為NaBr,同時說明M中X元素為Br元素,A能連續被氧化,說明A為醇,生成的D為酸,酸能和銀氨溶液發生銀鏡反應,說明D為HCOOH,則A為CH3OH、C為HCHO;
M中只含兩個O原子,且M屬于酯,說明M中含有酯基,根據 知,M為苯甲酸酯,而
知,M為苯甲酸酯,而 中的醛基是由兩個醇羥基失水形成的,則M中兩個-Br位于同一個C原子上,其結構簡式為
中的醛基是由兩個醇羥基失水形成的,則M中兩個-Br位于同一個C原子上,其結構簡式為 ,
, 和新制氫氧化銅懸濁液反應生成F,F結構簡式為
和新制氫氧化銅懸濁液反應生成F,F結構簡式為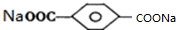 ,
, 酸化后再和氫氣發生加成反應生成E,根據E分子式知,E的結構簡式為
酸化后再和氫氣發生加成反應生成E,根據E分子式知,E的結構簡式為 ,據此分析解答.
,據此分析解答.
解答 解:M和氫氧化鈉的水溶液發生水解反應生成A、B和 ,B和硝酸酸化的硝酸銀溶液反應生成淡黃色沉淀AgBr,則B為NaBr,同時說明M中X元素為Br元素,A能連續被氧化,說明A為醇,生成的D為酸,酸能和銀氨溶液發生銀鏡反應,說明D為HCOOH,則A為CH3OH、C為HCHO;
,B和硝酸酸化的硝酸銀溶液反應生成淡黃色沉淀AgBr,則B為NaBr,同時說明M中X元素為Br元素,A能連續被氧化,說明A為醇,生成的D為酸,酸能和銀氨溶液發生銀鏡反應,說明D為HCOOH,則A為CH3OH、C為HCHO;
M中只含兩個O原子,且M屬于酯,說明M中含有酯基,根據 知,M為苯甲酸酯,而
知,M為苯甲酸酯,而 中的醛基是由兩個醇羥基失水形成的,則M中兩個-Br位于同一個C原子上,其結構簡式為
中的醛基是由兩個醇羥基失水形成的,則M中兩個-Br位于同一個C原子上,其結構簡式為 ,
, 和新制氫氧化銅懸濁液反應生成F,F結構簡式為
和新制氫氧化銅懸濁液反應生成F,F結構簡式為 ,
, 酸化后再和氫氣發生加成反應生成E,根據E分子式知,E的結構簡式為
酸化后再和氫氣發生加成反應生成E,根據E分子式知,E的結構簡式為 ,
,
(1)通過以上分析知,X為Br元素,反應①的反應類型是水解反應,
故答案為:Br;水解反應;
(2)通過以上分析知,M的結構簡式為: ,故答案為:
,故答案為: ;
;
(3)E為 ,E互為同分異構體同時符合下列四個條件
,E互為同分異構體同時符合下列四個條件
①含酯基,②含酚羥基,③不能發生銀鏡反應說明不是甲酸酯,④苯環上的一氯取代物只有2種,說明兩個取代基位于對位,符合條件的同分異構體有 、
、 ,
,
故答案為: 、
、 .
.
點評 本題考查有機物推斷,為高頻考點,側重考查學生分析推斷能力,正確推斷A的結構是解本題關鍵,注意結合題給信息解答,以D為突破口進行推斷,難點是(3)題同分異構體種類判斷.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol/L AgNO3溶液:H+、K+、SO42-、I- | |
| B. | 加入苯酚顯紫色的溶液:K+、NH4+、Cl-、I- | |
| C. | 甲基橙呈紅色的溶液中:MnO4-、Al3+、C2H5OH、SO42- | |
| D. | $\frac{{K}_{W}}{C({H}^{+})}$=0.1mol/L的溶液:K+、Na+、SiO32-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 手持試管給試管內的物質加熱 | |
| B. | 稀釋濃硫酸時,應將蒸餾水沿玻璃棒緩慢注入濃硫酸中 | |
| C. | 用天平稱量藥品時用手直接拿砝碼 | |
| D. | 用滴管滴加液體時滴管應垂直懸垂在容器上方且不能觸及容器內壁 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SiO2是酸性氧化物,不能與任何酸溶液反應 | |
| B. | 常溫下濃硫酸能使鋁發生鈍化,可在常溫下用鋁制容器貯運濃硫酸 | |
| C. | 測定中和反應的反應熱時,將堿緩慢倒入酸中,所測溫度值偏大 | |
| D. | 新制氯水顯酸性,向其中滴加少量紫色石蕊試液,充分振蕩后溶液呈紅色 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 元素編號 元素性質 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半徑 (10-10m) | 0.73 | 1.02 | 1.34 | 1.06 | 0.99 | 1.54 | 0.75 | 1.18 |
| 最高或最 低化合價 | +6 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -2 | -3 | -1 | -3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 醋酸鈉溶液可使酚酞試液變紅:CH3COO-+H2O?CH3COOH+OH- | |
| B. | NaHS水解:HS-+H2O═S2-+H3O+ | |
| C. | 向NaAlO2溶液中通入過量CO2:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- | |
| D. | 向AgCl的懸濁液中滴入少量Na2S溶液:2AgCl+S2-═Ag2S+2Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 鉛蓄電池放電時負極質量減少 | |
| B. | 在海輪外殼連接鎂合金保護外殼不受腐蝕 | |
| C. | 對于同一個化學反應,一步完成和分步完成其反應的焓變亦不相同 | |
| D. | 反應 MnO4-+H2O2+H+═Mn2++H2O+O2(未配平)中每生成1 mol O2轉移2 mol e- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 元素 | 有關信息 |
| X | 元素主要化合價為-2,原子半徑為0.074nm. |
| Y | 所在主族序數與所在周期序數之差為4. |
| Z | 原子半徑為0.102nm,核外最外層電子數是其電子層數的2倍,其單質在X的單質中燃燒,發出明亮的藍紫色火焰. |
| D | 最高價氧化物對應的水化物,能電離出離子數、電子數都相等的陰、陽離子. |
| E | 單質是生活中常見金屬,其制品在潮濕空氣中易被腐蝕或損壞. |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com