
���}Ŀ��һ���ض��£��ڹ̶��ݷe�����]�����аl(f��)�����з�����2HI(g)![]() H2(g)+I2(g)����HI�ĝ����0��1 mol L-1 ����0��07 mol L-1�r��Ҫ15s���tHI�ĝ����0��07 mol L-1����0��05 mol L-1�r������r�g��
H2(g)+I2(g)����HI�ĝ����0��1 mol L-1 ����0��07 mol L-1�r��Ҫ15s���tHI�ĝ����0��07 mol L-1����0��05 mol L-1�r������r�g��
A������15s B������10 s C������10s D����10 s

| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��������������W���ᡤ����(N��Bohr)����犐۵Ľ����Zؐ����������ˮ�ܽ�ɡ�����Һ�������W����ʽ�ɺ��α�ʾ�飺Au��HNO3��3HCl===AuCl3��NO����2H2O��AuCl3��HCl===HAuCl4(���ȺϽ���)���{����ӌ��@�N��Һ���ޱ�����ҕ����Ҋ�����o��֪����(zh��n)���Y��������W���ָ������·����������S���T�����ӠN���ZĿ�Ī��£�2HAuCl4![]() 2HCl����3Cl2����2Au�����F������ƌW�Ҍ�����ğo�ȟ�ۺͷǷ��ǻۡ����Д��������_����( )
2HCl����3Cl2����2Au�����F������ƌW�Ҍ�����ğo�ȟ�ۺͷǷ��ǻۡ����Д��������_����( )
A����ˮ���ܽ��S�𣬵������ܽ��
B��HAuCl4�����������
C���}���к���߀ԭ��
D�����}��͝����ᰴ���w�e��1��3�������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ�����W�����е����|׃��������׃��������׃�����������Ⱦ��ǻ��W�������о��ă��ݡ�
��1�����ڻ�Ԫ��������������һ���D����������ķ�����mA+nB![]() pC+qQ���f���䷴������v=k��cm��A��cn��B�������淴��Ҳ������Ƶı��_ʽ����k��ֻ�c�ض����P�����ʳ��������ڷǻ�Ԫ������������һ����ɵķ��������t���ʹ�ʽ�е�m��n�Ͳ�һ��������A��B�Ļ��WӋ��������ijһ���|���������ʟoӰ푣��t�䲻�����F��������ʽ�С�
pC+qQ���f���䷴������v=k��cm��A��cn��B�������淴��Ҳ������Ƶı��_ʽ����k��ֻ�c�ض����P�����ʳ��������ڷǻ�Ԫ������������һ����ɵķ��������t���ʹ�ʽ�е�m��n�Ͳ�һ��������A��B�Ļ��WӋ��������ijһ���|���������ʟoӰ푣��t�䲻�����F��������ʽ�С�
ij����С�M�y��������H2O2+2I+2H+![]() I2+H2O���IJ��������±���ʾ
I2+H2O���IJ��������±���ʾ
c��H2O2��/��mol��L1�� | c��I��/��mol��L1�� | c��H+��/��mol��L1�� | I2������������mol��L1��s1�� |
0.010 | 0.010 | 0.010 | 1.75 |
0.030 | 0.010 | 0.10 | 5.25 |
0.030 | 0.020 | 0.10 | 1.05 |
0.030 | 0.020 | 0.20 | 1.05 |
ԓ�����ķ��������c����Pϵ���_ʽ��_________________�����ʳ���k=____________��ԓ����_______����ǡ����ǡ�����Ԫ������
��2����������������ɴ����Ⱦ����Ҫ�ɷ�֮һ���ж�N�������������������Ⱦ������ ������������Ⱦ�ķ���֮һ��
��������2CO��g��+2NO��g��![]() N2��g��+2CO2��g�� ��H =746 kJ��mol1
N2��g��+2CO2��g�� ��H =746 kJ��mol1
��������CO��g��+NO2��g��![]() CO2��g��+ NO��g�� ��H=227 kJ��mol1
CO2��g��+ NO��g�� ��H=227 kJ��mol1
������CO��NO2߀ԭ����|�ğữ�W����ʽ ��
����֪C��O���I�ܞ�1076 kJ��mol1��C��O���I�ܞ�745 kJ��mol1���tʹ1 mol NO2��g����1 mol NO��g���ֽ��������ԭ������Ҫ������֮����___________��
��3����ij���]������ͨ������|������CO��NO����һ���l���°l(f��)�����·�����2CO��g��+2NO��g��![]() N2��g��+2CO2��g�� ��H =746 kJ��mol1���y�÷����ڲ�ͬ�ضȡ������l���£�ƽ��������CO2���w�e�֔���D1��ʾ����֪ԓ�������淴�����ʹ�ʽ��v��=
N2��g��+2CO2��g�� ��H =746 kJ��mol1���y�÷����ڲ�ͬ�ضȡ������l���£�ƽ��������CO2���w�e�֔���D1��ʾ����֪ԓ�������淴�����ʹ�ʽ��v��=
k��c2��CO2����c��N2�������y��ƽ��rv���cc��N2�����Pϵ��D2��ʾ��
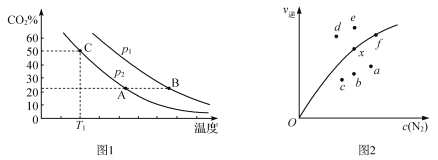
���D���У�A��B���c������ƽ�ⳣ��K��A��_________K��B����������������<������=������ͬ����p1_______p2��C�c�������ķ�����N2�Įa����_______________��
���D���У���x�c���ߵ�ijһ�ضȕr�����������_��ƽ�⣬�t׃?y��u)��������c��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��������������������M�������|���A��
��1���F���ǬF�����W���I(y��)�Ļ��A������M���ز����ٵĽ��ٲ��ϡ����I(y��)��ұ���F���ڟ��F�ߠt����һ����̼�������F߀ԭ������F����֪��
�� 2Fe��s��+ ![]() O2��g��=Fe2O3��s�� ��H=��824��6kJ/mol
O2��g��=Fe2O3��s�� ��H=��824��6kJ/mol
�� CO��g��+![]() O2��g��= CO2��g�� ��H=��283��0kJ/mol
O2��g��= CO2��g�� ��H=��283��0kJ/mol
Ո�������F�ߠt��ұ�F�ğữ�W����ʽ ��
��2���D��ʾһ���ض��£��A��Ͻ�M�����A���^�����v�S��ƽ��r���ĉ�����p�����M�S��ʾ�����К�ԭ���c����ԭ�ӂ����ȣ�H/M����������̎�ڈD��a�c�r�����֜ضȲ�׃��������wϵ��ͨ��������⣬�_��ƽ�������̎�ڈD�е�_____�c���b����c����d������10gԓ�Ͻ�2min�����՚��500mL����������v=______mLg-1min-1��

��3����������һ�N���ߜ��մɲ��ϡ��������Ȼ���͵����ښ���ձ��o�£��ӏ���l(f��)���������ɵ��^���ȵĵ����裬�����Ļ��W����ʽ��________��
��4���������@��NH4ClO4�������ڌ����ͻ���l(f��)�����M�����²��ϡ����y(t��ng)�Ƃ�NH4ClO4�ķ�����늽�NaClO3ˮ��Һ�õ�NaClO4�����cNH4Cl�M�Џͷֽⷴ�������ؽY���õ��֮aƷ���ಽ���ơ��ἃ�õ���NH4ClO4���½��о���һ�N�Ƃ��NH4ClO4���¹�ˇ��������������ö���늘O늽��HClO�õ���HClO4�����c����NH3�M�Ї��F�����Ƴɸ������@��
Ո�ش����І��}��
�������ɴ�����늽��Ƃ�������ꖘO늘O����ʽ�� ��
���c���y(t��ng)��ˇ��ȣ����J���¹�ˇ����Щ��(y��u)�c�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����1������׃���������ᷴ������______________(����̖)��
�������������w�ȱ�������CO2������Ȼ���ȼ�������џ�����ʯ����ϡ�}���cϡ��ˮ��ϣ�����ʯ���cˮ����������ʯ�ң��ɱ������A�����c�cˮ����������ʯ���c�Ȼ��@���w�ķ���
��2�����ȼ������Һ�B(t��i)ˮ�ğữ�W����ʽ��2H2(g)��O2(g)===2H2O(l) ��H����572 kJ��mol��1��Ո�ش����І��}��
����2 mol�����ȫȼ������ˮ���⣬�t�ų��ğ���______(����ڡ�����С�ڡ����ڡ�)572 kJ��
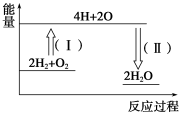
�ڷ���2H2��O2==2H2O������׃����D��ʾ����֪���_1 mol H2��1 mol O2��1 mol H��O�еĻ��W�I�քe��Ҫ����436 kJ��496 kJ��463 kJ�������t�����^��(��)___(����ա��ų���)___kJ������
��3����֪����2HI(g)==H2(g)��I2(g) ��H��+11 kJ��mol��1,1 mol H2(g)��1 mol I2(g)�����л��W�I���ѕr�քe��Ҫ����436 kJ��151 kJ���������t1 mol HI(g)�����л��W�I���ѕr�����յ�������____kJ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���D���ЌW���W�г�Ҋ�ЙC���D���Pϵ���������P���|�ͷ����l������ȥ��
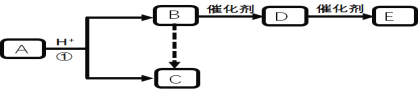
��֪������ C�����������|����60���ҷ�����̼Ԫ�ص��|���֔���40% ��
����B�� C��D���Ӻ�̼ԭ�ӂ�����ͬ��E��߷��ӻ����
�ش����І��}��
��1��B�к��еĹ��܈F���Q�� ��
��2��E��朹�(ji��)�� ��
��3�������������Ļ��W����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��������Ҫ�ķǽ���Ԫ�أ����|��;֮һ����ȡ���⣬��������ʽ�飺
N2(g)+3H2(g)![]() 2NH3(g)���ش����І��}��
2NH3(g)���ش����І��}��
��1����Ԫ����Ԫ�����ڱ���λ�Þ�______________��N2���Y��ʽ��______________
��2����һ���ݷe��2L�����]���������������������_ʼ�r�������|�����քe�飺n(N2)=2mol��n(H2)=4mol��2min��n(H2)=1mol��
v��ʾ�������ʣ��������_����______________
A��2minĩ�rn(NH3)=2.0molB��v(N2)=0.25mol��L��1��min��1
C��v(NH3)=1.0mol��L��1��min��1D��2minĩ�rN2�ĝ�Ȟ�0.5mol��L��1
��3����350�桢30MPa�ºϳɰ���r��n(NH3)��n(H2)(n��ʾ���|����)�S�r�g׃�����Pϵ���D��ʾ���������_����______________��
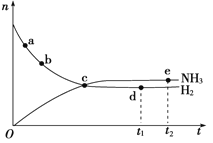
A���ca�����������ʱ��cb�Ĵ�
B���cc̎�����_��ƽ��
C���cd(t1�r��)���ce(t2�r��)̎n(N2)��һ��
D�������l����׃����������m����������ʹԓ�����ӿ�
��4���������γɶ�N�x�Ӻͷ��ӣ���N3-��NH2-��N2H4��N2H5+��N2H62+�ȣ���֪N2H5+��N2H62+�����Է���N2H4�Y���|�����ɵģ����cNH4+���Ƶ����|��
������N2H5+�c���A�������x�ӷ���ʽ�飺______________��
���ڻ�����M�����b��߀ԭ����(N2H4)�͏�������H2O2�����߷������ɃɷN����Ⱦ�h(hu��n)�������|������N2H4���ʽ______________��ԓ�����Ļ��W����ʽ��______________��
�������cN3-��Ӕ���ȵ�һ�N���ӵķ���ʽ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����2 L�ݷe��׃�������У��l(f��)��N2��3H2 ![]() 2NH3�ķ������Fͨ��4 mol H2��4 mol N2��10 s����H2��ʾ�ķ������ʞ�0.12 mol/(L��s)���t10 s��������N2�����|������
2NH3�ķ������Fͨ��4 mol H2��4 mol N2��10 s����H2��ʾ�ķ������ʞ�0.12 mol/(L��s)���t10 s��������N2�����|������
A. 1.6 mol B. 2.8 mol
C. 3.2 mol D. 3.6 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ�������W���x��3 ���|�Y���c���|��
���ڱ���ǰ������Ԫ��R��W��X��Y��Z��ԭ���������f����R���B(t��i)ԭ���У����ռ��������܌ӷ�̖��L������ܼ���ֻ�Ѓɂ�����������ͬ����ӡ����I(y��)��ͨ�^���xҺ�B(t��i)�՚�@��X���|��Yԭ�ӵ��������Ӕ��c��ӌӔ�֮�e����R��W��X���NԪ�ص�ԭ����֮�͡�Z���B(t��i)ԭ�ӵ������܌�ֻ��һ����ӣ������܌Ӿ��ѳ�M��ӡ�Ո�ش����І��}��
��1��Z2+���B(t��i)��������Ų�ʽ��________________��
��2��YX4-�Ŀ��g������_______���cYX4-���������w��һ�N���Ӟ�_______����Wʽ����HYX4���Ա�HYX2������ԭ����____________________��
��3���Y����ʽ��RX��W2H3��2�Ļ�������Rԭ�ӵ��s��܉����͞�_______��1molRX��W2H3��2�����к��Ц��I��Ŀ��_______________��
��4����Z�������}��Һ��ͨ���^����WH3��������[Z��WH3��4]SO4�������f�����_����_______��
A��[Z��WH3��4]SO4�������Ļ��W�I���x���I���O���I����λ�I
B����[Z��WH3��4]2+��Z2+�o������ӣ�WH3�ṩ��܉��
C��[Z��WH3��4]SO4�M��Ԫ���е�һ��x����������Ԫ��
��5��ijY�cZ�γɵĻ�����ľ�����D��ʾ�����c����Zԭ�ӣ���
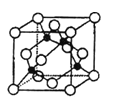
��ԓ���w�Ļ��Wʽ�� ��
����֪Z��Y���ؓ�Էքe��1.9��3.0���tY�cZ�γɵĻ�������� ����x�ӡ��������r���������
����֪ԓ���w���ܶȞ��g.cm��3�������ӵ��_������NA���tԓ���w��Zԭ�Ӻ�Yԭ��֮�g����̾��x�� pm��ֻ��Ӌ��ʽ����
�鿴�𰸺ͽ���>>
����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com