
分析 甲、乙、丙、丁分別是鹽酸、碳酸鈉、氯化鈣、硝酸銀4種溶液中的一種.將它們兩兩混合后,由復分解反應可知,只有硝酸銀與其它三種物質混合均生成白色沉淀,而只有碳酸鈉與鹽酸反應生成氣體,以此來解答.
解答 解:甲、乙、丙、丁分別是鹽酸、碳酸鈉、氯化鈣、硝酸銀4種溶液中的一種.將它們兩兩混合后,由復分解反應可知,只有硝酸銀與其它三種物質混合均生成白色沉淀,而只有碳酸鈉與鹽酸反應生成氣體,結合③丁與乙混合產生無色氣體,則丁、乙一定為鹽酸、碳酸鈉中的一種,②丙與乙或丁混合也產生沉淀,則丙為AgNO3;
①甲與乙或丙混合都產生沉淀,則甲為CaCl2,乙為Na2CO3,丁為HCl,
(1)丁與乙反應的離子方程式為CO32-+2H+=CO2↑+H2O,故答案為:CO32-+2H+=CO2↑+H2O;
(2)由上述分析可知,甲為CaCl2,乙為Na2CO3,丙為AgNO3,丁為HCl,故答案為:CaCl2;Na2CO3;AgNO3;HCl.
點評 本題考查無機物的推斷,為高頻考點,把握丙為硝酸銀及復分解反應的現象為解答的關鍵,側重分析與推斷能力的考查,注意元素化合物知識的綜合應用,題目難度中等.


科目:高中化學 來源: 題型:解答題
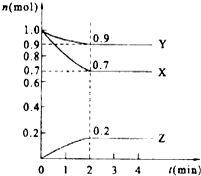 某溫度時,在2L的密閉容器中,X、Y、Z三種物質的量隨時間的變化曲線如圖所示.
某溫度時,在2L的密閉容器中,X、Y、Z三種物質的量隨時間的變化曲線如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 海水中含有鉀元素,只需經過物理變化就可以得到鉀單質 | |
| B. | 海水蒸發制海鹽的過程中發生了化學變化 | |
| C. | 利用潮汐發電是將化學能轉化為電能 | |
| D. | 從海水中可以得到NaCl,電解熔融NaCl可制備金屬鈉 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
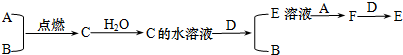
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氮氣化學性質不活潑,可用作食品防腐劑 | |
| B. | 硅膠無毒、無味、無腐蝕性,可用作食品干燥劑 | |
| C. | SiO2、Al2O3、MgO都有很高的熔點,可以制耐火材料 | |
| D. | 二氧化錳具有強氧化性,可用作H2O2分解的氧化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:1 | B. | 2:3 | C. | 3:4 | D. | 4:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
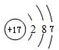 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com