
【題目】工業上用洗凈的廢銅屑作原料來制備硝酸銅。為了節約原料和防止污染環境,宜采取的方法( )
A.![]()
B.![]()
C.![]()
D.![]()
【答案】B
【解析】
試題分析: A.Cu+2H2SO4(濃)![]() CuSO4+SO2↑+2H2O、CuSO4+Ba(NO3)2=BaSO4↓+Cu(NO3)2,該過程中生成有毒氣體二氧化硫且浪費濃硫酸、硝酸鋇,所以不符合條件,故A不選;B.2 Cu+O2
CuSO4+SO2↑+2H2O、CuSO4+Ba(NO3)2=BaSO4↓+Cu(NO3)2,該過程中生成有毒氣體二氧化硫且浪費濃硫酸、硝酸鋇,所以不符合條件,故A不選;B.2 Cu+O2![]() 2CuO、CuO+2HNO3=Cu(NO3)2+H2O,該反應中沒有有毒氣體生成,且能節約硝酸,所以符合條件,故B選;C.3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,NO有毒會污染環境,所以不符合條件,故C不選;D.Cu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2O,二氧化氮有毒而污染環境,所以不符合條件,故D不選;故選B。
2CuO、CuO+2HNO3=Cu(NO3)2+H2O,該反應中沒有有毒氣體生成,且能節約硝酸,所以符合條件,故B選;C.3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,NO有毒會污染環境,所以不符合條件,故C不選;D.Cu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2O,二氧化氮有毒而污染環境,所以不符合條件,故D不選;故選B。


科目:高中化學 來源: 題型:
【題目】I、某化學興趣小組利用以下裝置模擬合成氨并制備少量氨水

已知:加熱(85℃)NH4Cl和NaNO2飽和溶液可以制取N2
B中儀器名稱是___________________;
⑵為了完成實驗,裝置從左到右接口的連接順序是_____![]() ______;
______;
⑶D中玻璃纖維的作用是_________________;
⑷小組中甲同學認為F裝置不太合理,實驗中會產生倒吸。乙同學認真分析后認為該裝置無需改進,他的理由是________________________;
II、實驗探究
⑸該小組同學利用制備的氨水再進行銀鏡反應實驗。經查閱資料,配制的銀氨溶液主要成分是[Ag(NH3)2]OH,小組同學對其組成進行了如下實驗探究:
①在潔凈的小試管中加入2mL 2%的AgNO3溶液,然后邊振蕩試管邊滴加2%的稀氨水溶液,至最初產生的沉淀恰好溶解為止,制得銀氨溶液。
②在制得的銀氨溶液中加入無水乙醇,溶液變渾濁,過濾,用__________洗滌,得到白色固體;
③將該白色固體用適量蒸餾水溶解,得到無色溶液,用廣范pH試紙檢驗溶液近似呈中性;向溶液中逐滴加入稀鹽酸至不再產生沉淀,靜置,取上層清液于另一支放有一小片銅的小試管中并微熱,發現銅片的表面有氣泡產生,遇到空氣變成紅棕色;另取少量上層清液加過量的NaOH溶液并加熱,得到無色刺激性氣體。由此確定通過上述方法制備的白色固體主要成分是___________________;
⑹請根據以上探究,設計實驗來制備少量純凈的[Ag(NH3)2]OH溶液:取2mL 2%的AgNO3溶液于潔凈的小試管中,_________________,即得到[Ag(NH3)2]OH溶液。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關電解質溶液的說法正確的是( )
A.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中![]() 減小
減小
B.稀醋酸中加入少量醋酸鈉能增大醋酸的電離程度
C.稀醋酸中加入少量NaOH固體,溶液的導電性增強
D.向醋酸中加入氨水至中性,溶液中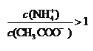
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據下列有關圖象,說法正確的是( )
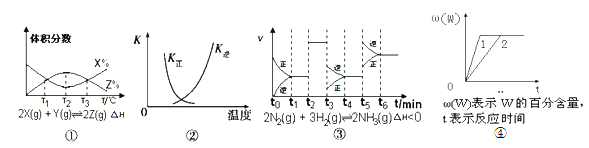
A. 由圖①知,反應在T1、T3處達到平衡,且該反應的△H<0
B. 圖②中曲線表示反應2SO2(g)+O2(g) ![]() 2SO3(g),ΔH<0的正、逆反應平衡常數K隨溫度的變化
2SO3(g),ΔH<0的正、逆反應平衡常數K隨溫度的變化
C. 由圖③知,反應在t6時,NH3體積分數最大。
D. 其他條件不變時,圖④中曲線表示不同壓強對反應aX(g)+bY(s)![]() nW(g)的影響,且P1>P2,n=a+b。
nW(g)的影響,且P1>P2,n=a+b。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將4 mol A氣體和2 mol B氣體充入2 L的密閉容器中,一定條件下發生如下反應:2A(g)+B(g)![]() 2C(g)。若經2 s后測得C的濃度為0.6 mol ·L-1,下列幾種說法正確的是
2C(g)。若經2 s后測得C的濃度為0.6 mol ·L-1,下列幾種說法正確的是
①用物質A表示的反應平均速率為0.3 mol ·L-1·s-1
②用物質B表示的反應的平均速率為0.6 mol ·L-1·s-1
③2 s時物質A的轉化率為70%
④2 s時物質B的濃度為0.7 mol ·L-1
A. ①③ B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25 ℃時,濃度均為0.1mol/L的下列五種鈉鹽溶液的pH如下表:
溶質 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
回答下列問題:
(1)下列反應不能發生的是: ;
a.CO32-+CH3COOH=CH3COO-+CO2↑+H2O
b.ClO-+CH3COOH=CH3COO-+HClO
c.CO32-+HClO=CO2↑+H2O+ClO-
d.2ClO-+CO2+H2O=CO32-+2HClO
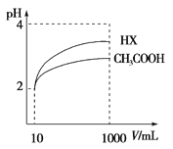
(2)體積為10 mL pH=2的醋酸溶液與一元酸HX分別加水稀釋至1000mL,稀釋過程pH變化如右上圖,則HX的電離平衡常數________(填“大于”、“等于”或“小于”)醋酸的平衡常數,寫出HX的電離方程式 。
(3)某溫度下,純水中c (H+)=2.0×10-7 mol·L1, 0.9mol·L-1NaOH溶液與0.1mol·L-1HCl溶液等體積混合后(不考慮溶液體積變化),溶液的pH= 。
(4)等濃度等體積的CH3COONa和NaCN混合后,所得混合溶液中各離子濃度的大小關系是: 。
(5)某二元酸H2B在水中的電離方程式為H2B = H+ + HB— ;HB—![]() H++ B2—,則NaHB溶液顯 (填“酸性”、“中性”或“堿性”)。
H++ B2—,則NaHB溶液顯 (填“酸性”、“中性”或“堿性”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】4種短周期元素W、X、Y、Z的原子序數依次增大,其原子的最外層電子數之和為19,W和X元素原子內質子數之比為1:2,X2+和Z-離子的電子數之差為8,下列說法不正確的是 ( )
A. 與W相鄰的同主族元素可制成重要的半導體材料
B. X單質不可能置換出W單質
C. 元素原子半徑從大到小的順序是X、Y、Z
D. W、Y、Z元素最高價氧化物對應的水化物中酸性最強的是HZO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于![]() 的說法正確的是( )
的說法正確的是( )
A.所有碳原子有可能都在同一平面上
B.最多只可能有9個碳原子在同一平面上
C.有7個碳原子可能在同一直線上
D.至少有6個碳原子在同一直線上
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“納米材料”是指直徑從幾納米至幾十納米的材料,目前已廣泛應用于催化劑及軍事技術中,如果將納米材料分散到液體分散劑中,所得混合物
A.不能透過濾紙 B.一定是濁液
C.一定是溶液 D.有丁達爾效應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com