
分析 (1)①水泥的原料是粘土和石灰石,玻璃的原料是純堿、石灰石和石英,所以原料中均有石灰石;
②橡膠有天然的和人工合成的,都是高分子材料;
③鋼鐵是鐵的合金易發生電化學腐蝕;正極上氧氣得電子;
(2)①PM2.5”是指大氣層中直徑≥2.5μm的顆粒物,能被肺吸收并進入血液,對人體危害很大,是形成霧霾的主要污染物;
②不能燃燒的垃圾,不能采用焚燒處理;
③混凝劑適用于除去廢水中的懸浮物;沉淀法適用于除去廢水中的重金屬離子;中和法適用于除去廢水中的酸;
④氯氣和石灰乳反應生成氯化鈣、次氯酸鈣、水;
(3)①蔬菜中富含維生素C;
②碘元素被稱為智力元素;
③蛋白質水解生成氨基酸,蛋白質能發生鹽析;
④部分抗生素會產生不良反應要做皮試.
解答 解:(1)①生產玻璃的原料是純堿、石灰石和石英,高溫下,碳酸鈉、碳酸鈣和二氧化硅反應分別生成硅酸鈉、硅酸鈣;
生產水泥以黏土和石灰石為主要原料,經研磨、混合后在水泥回轉窯中煅燒,再加入適量石膏,并研成細粉就得到普通水泥;所以在玻璃工業、水泥工業中都用到的原料是石灰石,故答案為:石灰石(或CaCO3);
②橡膠分為天然橡膠和合成橡膠,天然橡膠的成分是聚異戊二烯 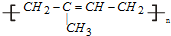 ,合成橡膠主要指:順丁橡膠、氯丁橡膠、丁苯橡膠等,都為有機高分子材料,故答案為:c;
,合成橡膠主要指:順丁橡膠、氯丁橡膠、丁苯橡膠等,都為有機高分子材料,故答案為:c;
③鋼鐵是鐵的合金在潮濕的空氣中易發生吸氧腐蝕;正極上氧氣得電子被還原,其電極反應為:O2+4e-+2H2O=4OH-;
故答案為:吸氧;O2+4e-+2H2O=4OH-;
(2)①導致霧霾形成的主要污染物是pM2.5,能被肺吸收并進入血液,對人體危害很大,故選c;
②電池中的重金屬能污染環境,所以不能隨意丟棄電池,廢棄塑料不能焚燒,否則會導致環境污染,產生大量有害氣體;
故答案為:ac;
③a.和法適用于除去廢水中的酸,所以用中和法除去廢水中的酸,故a正確;
b.用沉淀法除去廢水中的重金屬離子,故b錯誤;
c.用混凝劑如明礬等除去廢水中的懸浮物,氯氣能消毒殺菌,但不能除去懸浮物,故c錯誤;
故答案為:a;
④氯氣和石灰乳反應生成氯化鈣、次氯酸鈣、水,該反應為2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,故答案為:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(3)①蔬菜中富含維生素C,所以富含維生素C的是辣椒,故答案為:b;
②碘元素被稱為智力元素,缺乏碘元素將導致甲狀腺腫大,且造成智力損害,故答案為:a;
③蛋白質在一定條件下水解生成氨基酸,在蛋白質溶液中加入飽和硫酸銨溶液能發生鹽析,即有白色沉淀析出,故答案為:氨基酸;鹽析;
④部分抗生素會產生不良反應要做皮試,所以使用青霉素前使用者一定要進行皮膚敏感試驗,故答案為:皮試.
點評 本題考查常見的環境污染物、漂白粉的制備和藥物的主要成分和療效等,為高頻考點,難度不大,注意知識的積累,本題注重化學與生活的聯系,明確化學服務于生活,學會利用化學知識解決生活中的問題.


 智趣暑假溫故知新系列答案
智趣暑假溫故知新系列答案 英語小英雄天天默寫系列答案
英語小英雄天天默寫系列答案 暑假作業安徽少年兒童出版社系列答案
暑假作業安徽少年兒童出版社系列答案科目:高中化學 來源: 題型:選擇題
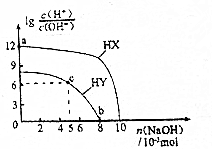
| A. | HX的酸性弱于HY | |
| B. | a點由水電離出的c(H+)=10-12mol•L-1 | |
| C. | c點溶液中:c(Y-)>c(HY) | |
| D. | b點時酸堿恰好完全中和 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 乙池中CuSO4溶液的濃度不變 | |
| B. | 甲池中理論上消耗標準狀況下空氣的體積是2.8L(空氣中O2體積分數以20%計算) | |
| C. | 甲池是電能轉化為化學能的裝置,乙池是化學能轉化為電能的裝置 | |
| D. | 甲池中通入CH3OH一極的電極反應為CH3OH-6e-+2H2O═CO32-+8H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| A元素的核外電子數和電子層數相等 |
| B元素原子的核外p電子數比s電子數少1 |
| C原子的第一至第四電離能如下: |
| I1=738kJ•mol-1 I2=1451kJ•mol-1 I3=7733kJ•mol-1 I4=10540kJ•mol-1 |
| D原子核外所有p軌道全滿或半滿 |
| E元素的主族序數與周期數的差為4 |
| F是前四周期中電負性最小的元素 |
| G在周期表的第七列 |
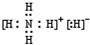 .
.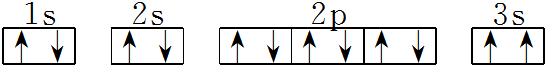 該同學所畫的電子排布圖違背了泡利原理.
該同學所畫的電子排布圖違背了泡利原理.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 1mol NH4+和1mol OH-所含電子數均為10NA | |
| B. | 14gC2H4和14gC3H6 所含原子數均為3NA | |
| C. | 1L l mol/LH2SO4溶液與足量Zn充分反應生成22.4L H2 | |
| D. | 標準狀況下,11.2LSO3所含分子數為0.5NA |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
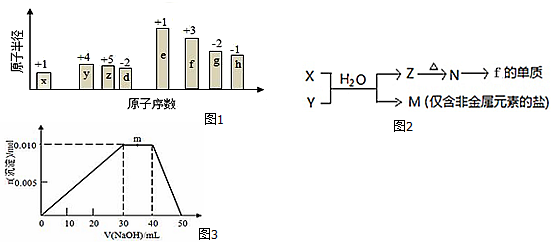
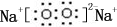 ;B是常見的液態化合物,其稀溶液易被催化分解,可使用的催化劑為AB.(填序號)
;B是常見的液態化合物,其稀溶液易被催化分解,可使用的催化劑為AB.(填序號)查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com