
| A. | 標準狀況下,22.4L CHCl3含氯原子數為3NA | |
| B. | 100mL 1 mol•L-1醋酸溶液中的氫原子數為0.4NA | |
| C. | 常溫常壓下,11.2g乙烯中共用電子對數為2.4NA | |
| D. | 6.4 g CaC2晶體中所含的離子總數為0.3NA |
分析 A.標準狀況下,CHCl3不是氣體;
B.醋酸在水中發生電離生成氫離子;
C.根據乙烯的結構計算出含有的共用電子對數目;
D.CaC2晶體中含有陰離子為C22-,陽離子為Ca2+.
解答 解:A.標準狀況下,CHCl3不是氣體,因此無法計算22.4L CHCl3含氯原子數,故A錯誤;
B.100mL 1 mol•L-1醋酸溶液中溶質的物質的量為0.1mol,醋酸在水中發生電離生成氫離子,因此氫原子數小于0.4NA,故B錯誤;
C.11.2g乙烯的物質的量為:$\frac{11.2g}{28g/mol}$=0.4molmol,含有1.6mol碳氫鍵和0.4mol碳碳鍵,總共含有2.4mol共用電子對,含有共用電子對數目為2.4NA,故C正確;
D.CaC2晶體的物質的量為$\frac{6.4g}{64g/mol}$=0.1mol,晶體中含有陰離子為C22-,陽離子為Ca2+,則晶體中含有陰陽離子總數為0.2NA,故D錯誤;
故選C.
點評 本題考查了考查阿伏加德羅常數的有關計算和判斷,題目難度中等,注意標準狀況下CHCl3的狀態不是氣體,阿伏加德羅常數是歷年高考的“熱點”問題,這是由于它既考查了學生對物質的量、粒子數、質量、體積等與阿伏加德羅常數關系的理解,又可以涵蓋多角度的化學知識內容.


科目:高中化學 來源: 題型:解答題
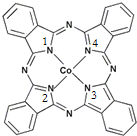 鈷(Co)是人體必需的微量元素.含鈷化合物作為顏料,具有悠久的歷史,在機械制造、磁性材料等領域也具有廣泛的應用.請回答下列問題:
鈷(Co)是人體必需的微量元素.含鈷化合物作為顏料,具有悠久的歷史,在機械制造、磁性材料等領域也具有廣泛的應用.請回答下列問題: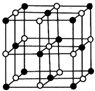 ,在該晶體中與一個鈷原子等距離且最近的鈷原子有12個;筑波材料科學國家實驗室一個科研小組發現了在 5K 下呈現超導性的晶體,該晶體具有CoO2的層狀結構(如下圖所示,小球表示Co原子,大球表示O原子).下列用粗線畫出的重復結構單元示意圖不能描述CoO2的化學組成的是D.
,在該晶體中與一個鈷原子等距離且最近的鈷原子有12個;筑波材料科學國家實驗室一個科研小組發現了在 5K 下呈現超導性的晶體,該晶體具有CoO2的層狀結構(如下圖所示,小球表示Co原子,大球表示O原子).下列用粗線畫出的重復結構單元示意圖不能描述CoO2的化學組成的是D.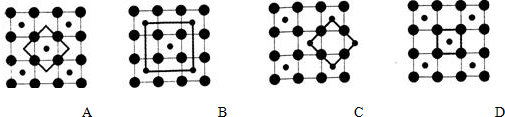
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
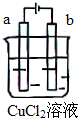
| A. | 電極a表面呈紅色 | |
| B. | 電極b表面有氣泡生成 | |
| C. | 電子由電源的負極沿導線流向電極b | |
| D. | 該裝置能量轉化形式為化學能轉化為電能 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.4mol/L | B. | 0.2mol/L | C. | 0.1mol/L | D. | 0.08mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
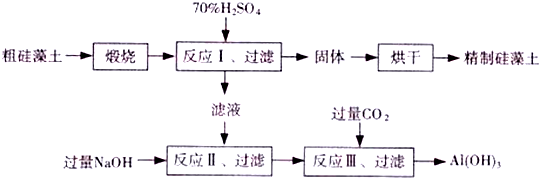
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | ①②③均屬于氧化還原反應 | B. | H2和HCl均可循環利用 | ||
| C. | SiO2是一種堅硬難熔的固體 | D. | 硅可用于制作光導纖維 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com