
 定樣品中Na2O2的含量.
定樣品中Na2O2的含量.
| m樣品 | m難溶雜質 | m(NaCl) |
| 8.00g | 0.42g | 10.53g |
分析 (1)根據提供的藥品,結合中學化學所學內容,可以探究鐵罐內的試劑是否變質;
(2)根據物質的顏色可初步推斷物質的種類;
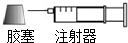
(3)方法1:根據量氣法原理可知,先要準確稱取一定量的樣品,置于注射器中,再在注射器中吸入足量的水,立即用膠塞堵住針頭,防止產生的氧氣逸出,使過氧化鈉與水反應,平放注射器,使注射器內外壓強一致,準確讀數,根據注射器上的讀數可知氧氣的體積,據此進行計算;
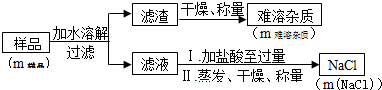
方法2:將樣品溶解、過濾得濾液和濾渣,濾渣為難溶性雜質,根據雜質的質量可知樣品中Na2O2和Na2CO3的質量,濾液中為氫氧化鈉和碳酸鈉,與足量的鹽酸反應得氯化鈉,蒸發、干燥、稱量后得氯化鈉的質量,根據所得氯化鈉的質量和樣品中Na2O2和Na2CO3的質量列方程組可求得過氧化鈉的質量,在這一方法中溶解、過濾、蒸發都用到玻璃棒;
(4)方法2中首先設樣品中含鈉元素的物質只有Na2O2和Na2CO3,而事實上不一定是這樣的組成,也可能有氧化鈉或碳酸氫鈉等,如果有這些物質,則根據上面列方程組解得提過氧化鈉的質量就不準確了,據此答題.
解答 解:(1)根據提供的藥品,結合中學化學所學內容,可以探究鐵罐內的試劑是否變質,故答案為:探究試劑是否變質;
(2)過氧化鈉為淡黃色粉末,如果瓶內固體的顏色為白色,則可初步說明過氧化鈉已經變質,故答案為:淡黃;
(3)方法1:根據量氣法原理可知,先要準確稱取一定量的樣品,置于注射器中,再在注射器中吸入足量的水,立即用膠塞堵住針頭,防止產生的氧氣逸出,使過氧化鈉與水反應,平放注射器,使注射器內外壓強一致,準確讀數,根據注射器上的讀數可知氧氣的體積,據此進行計算,所以A操作為稱量,B操作為用膠塞迅速堵住針頭,C操作為讀數,
故答案為:稱量;膠塞;讀數;
方法2:將樣品溶解、過濾得濾液和濾渣,濾渣為難溶性雜質,根據雜質的質量可知樣品中Na2O2和Na2CO3的質量,濾液中為氫氧化鈉和碳酸鈉,與足量的鹽酸反應得氯化鈉,蒸發、干燥、稱量后得氯化鈉的質量,根據所得氯化鈉的質量和樣品中Na2O2和Na2CO3的質量列方程組可求得過氧化鈉的質量,
①在這一方法中溶解、過濾、蒸發都用到玻璃棒,
故答案為:溶解;過濾、蒸發;
②濾液中為氫氧化鈉和碳酸鈉,往濾液中加稀鹽酸至過量,其目的是使濾液中的NaOH、Na2CO3完全轉化為NaCl,故答案為:NaOH、Na2CO3;
③往難溶雜質中滴加稀鹽酸,發現其溶解,所得溶液呈黃色,說明樣品中的難溶雜質為Fe2O3,故答案為:Fe2O3;
④根據表中的數據可知,品中Na2O2和Na2CO3的質量為8.00g-0.42g=7.58g,設樣品中Na2O2的物質的量為xmol,Na2CO3的物質的量為ymol,則$\left\{\begin{array}{l}{2(x+y)×58.5=10.53}\\{78x+106y=7.58}\end{array}\right.$,解得x=0.068,y=0.021,所以Na2O2的質量分數為$\frac{78×0.068}{8}$×100%=66.3%,
故答案為:66.3%;
(4)方法2中首先設樣品中含鈉元素的物質只有Na2O2和Na2CO3,而事實上不一定是這樣的組成,也可能有氧化鈉或碳酸氫鈉等,如果有這些物質,則根據上面列方程組解得提過氧化鈉的質量就不準確了,而方法1中只有過氧化鈉與水反應產生氧氣,所以方法1的測量結果更準確,
故答案為:1.
點評 本題考查了物質組成的定量實驗,實驗過程的設計方法,產物實驗驗證的設計方法和現象判斷,掌握基礎是關鍵,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | AlCl3溶液中加入過量氨水:Al3++4NH3•H2O═AlO${\;}_{2}^{-}$+4NH${\;}_{4}^{+}$+2H2O | |
| B. | 在海帶灰的浸出液(含有I-)中滴加H2O2得到I2:2I-+H2O2+2H+═I2+O2↑+2H2O | |
| C. | 在氫氧化鋇溶液中滴加硫酸氫鉀溶液至PH=7:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 用碳酸鈉溶液浸泡鍋爐水垢:Ca2++CO32-═CaCO3↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 它有利于兒童牙齒的生長 | |
| B. | 它有利于骨骼的生長和發育 | |
| C. | 它有利于化合物Ca10(PO4)6(OH)2的生成 | |
| D. | 它使兒童更聰明 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③ | B. | ② | C. | ①② | D. | ②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度/℃ | 400 | 500 | 800 |
| 平衡常數K | 9.94 | 9 | 1 |
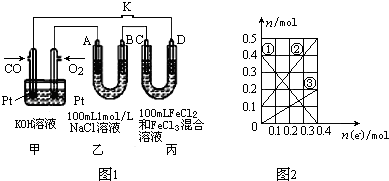
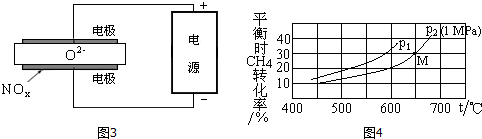
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | X2+是XO4-的還原產物 | |
| B. | 溶液中可發生:Z2+2A2+═2A3++2Z- | |
| C. | 氧化性強弱的順序為:XO4->B2>Z2>A3+ | |
| D. | Z2在①中是氧化產物,③中是氧化劑 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com