
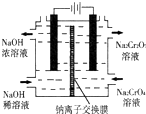
 (1)已知在常溫常壓下:
(1)已知在常溫常壓下:| 實驗組 | 溫度℃ | 起始量/mol | 平衡量/mol | 達到平衡所需 時間/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
 ),聚丙烯酸鈉單體的結構簡式是
),聚丙烯酸鈉單體的結構簡式是
| ||||
|
| 1 |
| 6 |
| a |
| b |
| a |
| b |
| ||||
|


 同步輕松練習系列答案
同步輕松練習系列答案 課課通課程標準思維方法與能力訓練系列答案
課課通課程標準思維方法與能力訓練系列答案科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
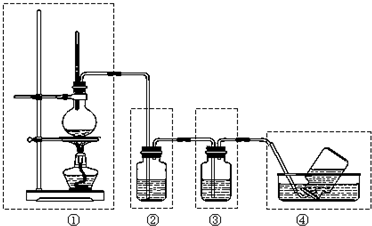
查看答案和解析>>
科目:高中化學 來源: 題型:
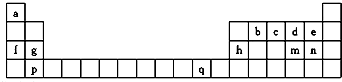
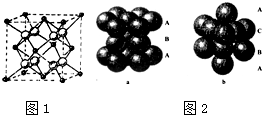
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、用托盤天平直接稱量燒堿4.0g |
| B、在蒸發皿中灼燒CuSO4?5H2O晶體以除去結晶水 |
| C、用標準鹽酸溶液滴定未知濃度的氨水,用酚酞作指示劑 |
| D、配制0.9%的氯化鈉溶液時,將稱量的氯化鈉放入燒杯中加計量的水攪拌溶解 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com