
分析 (1)該反應中C元素化合價由0價變為+4價、S元素化合價由+6價變為+4價,所以C作還原劑、濃硫酸作氧化劑;
有2mol濃硫酸參加反應時消耗12gC,根據濃硫酸和C之間的關系式計算消耗C的質量;
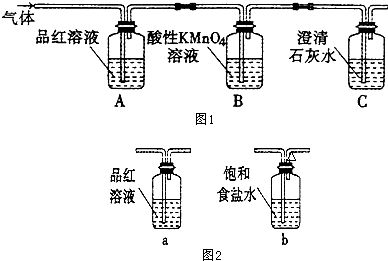
(2)二氧化硫具有漂白性,能使品紅溶液褪色;
(3)二氧化硫具有還原性,能被強氧化劑高錳酸鉀溶液氧化而使酸性高錳酸鉀溶液褪色;
(4)二氧化碳屬于酸性氧化物,能和氫氧化鈣反應生成難溶性白色固體碳酸鈣;
(5)二氧化硫能使品紅溶液褪色,所以用品紅溶液檢驗二氧化硫;
(6)二氧化硫是形成酸雨的主要成分;二氧化碳是造成溫室效應的氣體.
解答 解:(1)該反應中C元素化合價由0價變為+4價、S元素化合價由+6價變為+4價,所以C作還原劑、濃硫酸作氧化劑;
有2mol濃硫酸參加反應時消耗12gC,若有0.2mol的H2SO4完全參加反應,則消耗碳的質量是1.2g,
故答案為:氧化劑;1.2;
(2)二氧化硫具有漂白性,能使品紅溶液褪色,氣體中含有二氧化硫,所以氣體通入A裝置,看到的現象是品紅溶液褪色,故答案為:褪色;二氧化硫;
(3)二氧化硫具有還原性,能被強氧化劑高錳酸鉀溶液氧化而使酸性高錳酸鉀溶液褪色,所以B裝置目的是吸收二氧化硫,故答案為:吸收二氧化硫;
(4)二氧化碳屬于酸性氧化物,能和氫氧化鈣反應生成難溶性白色固體碳酸鈣,所以C中看到的現象是產生白色沉淀,故答案為:白色;
(5)二氧化硫能使品紅溶液褪色,所以用品紅溶液檢驗二氧化硫,故選a;
(6)二氧化硫是形成酸雨的主要成分;二氧化碳是造成溫室效應的氣體,
故選A;C.
點評 本題考查性質實驗方案評價,為高頻考點,明確實驗原理及物質性質是解本題關鍵,知道二氧化硫檢驗方法及性質,注意:二氧化硫、二氧化碳都能使澄清石灰水變渾濁,題目難度不大.


科目:高中化學 來源: 題型:解答題
| 化學反應 | 能量轉化形式 |
| ①CH4+2O2$\frac{\underline{\;點燃\;}}{\;}$CO2+2H2O | 由 化學能轉化為 熱能 |
| ②Pb+PbO2+2H2SO4$?_{充電}^{放電}$2PbSO4+2H2O | 由 化學能轉化為 電能 |
| ③CaCO3$\frac{\underline{\;高溫\;}}{\;}$Ca+CO2↑ | 由 熱能轉化為 化學能 |
| ④6nH2O+6nCO2$→_{葉綠素}^{光}$(C6H12O6)n+6nO2 | 由 光能轉化為 化學能 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 溫度/℃ | 200℃ | 250℃ | 300℃ |
| 平衡常數/(mol•L-1)2 | K1 | K2 | 80 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
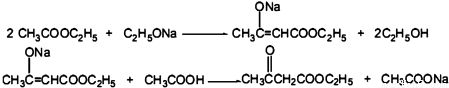

 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 與
與
 與
與
 與
與
 與
與
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
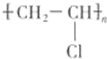 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com