
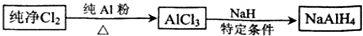
分析 (1)鋁氫化鈉遇水發生劇烈反應產生偏鋁酸鈉和氫氣,據此書寫方程式;
(2)NaCl是離子化合物,和有機物之間互不相溶,所以反應生成的氯化鈉沉淀在氫化鈉表面,阻止了氯化鋁和氫化鈉進一步反應,據此回答;
(3)氯化鋁的制備是金屬鋁和氯氣之間反應的產物,濃鹽酸和高錳酸鉀(氯酸鉀或重鉻酸鉀)之間無條件的反應產物是氯氣,但是金屬鋁易被氧氣氧化而變質,所以點燃D處酒精燈之前需排除裝置中的空氣;
(4)金屬鈉和氫氣之間化合可以得NaH,但是氫氣中的氯化氫要除去,金屬鈉和氧氣加熱下會產生過氧化鈉雜質,據此回答;
(5)由反應原理得,測定鋁氫化鈉樣品的純度即通過測定鋁氫化鈉與水反應生成的氫氣的量計算鋁氫化鈉的量,從而計算其純度.
解答 解:(1)鋁氫化鈉遇水發生劇烈反應產生偏鋁酸鈉和氫氣,其反應的化學方程式為NaAlH4+2H2O=NaAlO2+4H2↑,故答案為:NaAlH4+2H2O=NaAlO2+4H2↑;
(2)AlCl3與NaH反應時,需將AlCl3溶于有機溶劑,再將得到的溶液滴加到NaH粉末上,則生成的NaCl是離子化合物,和有機物之間互不相溶,所以反應生成的氯化鈉沉淀在氫化鈉表面,阻止了氯化鋁和氫化鈉進一步反應,導致NaH的轉化率較低,故答案為:反應生成的氯化鈉沉淀在氫化鈉表面,阻止了氯化鋁和氫化鈉進一步反應;
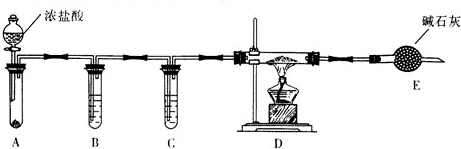
(3)①氯化鋁的制備是金屬鋁和氯氣之間反應的產物,則裝置A為制備氯氣的發生裝置,濃鹽酸和高錳酸鉀(氯酸鉀或重鉻酸鉀)之間無條件的反應產物是氯氣,所以A中所盛裝的試劑的名稱為高錳酸鉀(氯酸鉀或重鉻酸鉀),故答案為:高錳酸鉀(氯酸鉀或重鉻酸鉀);
②因為金屬鋁易被氧氣氧化而變質,所以點燃D處酒精燈之前需排除裝置中的空氣,即打開分液漏斗的活塞使A中發生反應,待D中充滿黃綠色的氣體時點燃酒精燈,故答案為:打開分液漏斗的活塞使A中發生反應,待D中充滿黃綠色的氣體時點燃酒精燈;
(4)制取NaH則用金屬鈉和氫氣化合可以得到,所以A裝置為氫氣的發生裝置,B為除去氫氣中的HCl氣體,所以用氫氧化鈉溶液,而原來是除去氯氣中的HCl用的是飽和食鹽水;又由于裝置中會有空氣殘留,所以金屬鈉和氧氣加熱下會產生過氧化鈉雜質,再加上有鈉剩余,則如果操作不當,制得的NaH中可能含有Na、Na2O2,故答案為:飽和食鹽水;氫氧化鈉溶液;Na、Na2O2;
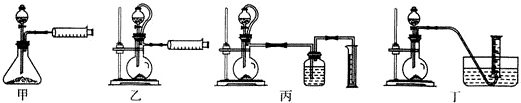
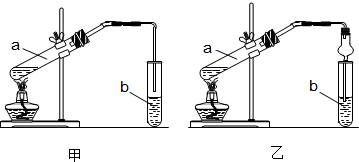
(5)由反應原理得,測定鋁氫化鈉樣品的純度即通過測定鋁氫化鈉與水反應生成的氫氣的量計算鋁氫化鈉的量,從而計算其純度,所以從簡約性、準確性考慮,最甲沒有使用恒壓漏斗,測出的氫氣有誤差;C、D采用排水法收集氫氣,由于導管中會有殘留,導致測出的氫氣有誤差,適宜的方案是乙;通過連續兩次讀數的氫氣體積相等,說明鋁氫化鈉與水完全反應,冷卻至室溫,故答案為:乙;連續兩次讀數的氫氣體積相等.
點評 本題考查知識點較多,涉及方程式的書寫、裝置圖的選擇、物質的制備和除雜等元素化合物的性質,屬于拼合型題目,需要學生具備扎實的基礎,難度中等.


 中考解讀考點精練系列答案
中考解讀考點精練系列答案科目:高中化學 來源:2016-2017學年寧夏衛一高一上10月月考化學a卷(解析版) 題型:填空題
完成下列表格(注明單位):
微粒 | 摩爾質量 | 質量 | 物質的量 | 微粒數 |
O | 16g/mol | 16g | ||
N2 | 0.5mol | |||
Cu | 64g/mol | 2NA | ||
H2SO4 | 1.5NA |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年安徽師大附中高二上10月月考化學卷(解析版) 題型:選擇題
模型法是化學中把微觀問題宏觀化的最常見方法,對于反應2HBr(g) H2(g)+Br2(g),下列四個圖中可以表示該反應在一定條件下為可逆反應的是
H2(g)+Br2(g),下列四個圖中可以表示該反應在一定條件下為可逆反應的是
A.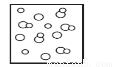 B.
B.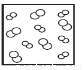 C.
C.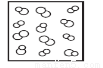 D.
D.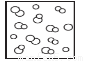
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
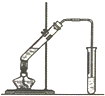 Ⅰ.乙烯是石油裂解氣的主要成分,乙烯的結構簡式為H2C=CH2.
Ⅰ.乙烯是石油裂解氣的主要成分,乙烯的結構簡式為H2C=CH2.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
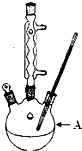 苯甲酸廣泛應用于制藥和化工行業,某興趣小組同學利用高錳酸鉀氧化甲苯制備苯甲酸(KMnO4中性條件下還原產物為MnO2,酸性條件下為Mn2+)
苯甲酸廣泛應用于制藥和化工行業,某興趣小組同學利用高錳酸鉀氧化甲苯制備苯甲酸(KMnO4中性條件下還原產物為MnO2,酸性條件下為Mn2+)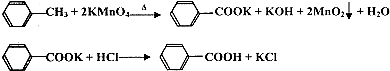
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 體積(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 化學鍵 | H-O | O=O |
| 鍵能/KJ?mol-1 | 463.4 | 498 |
| A. | 413KJ/mol | B. | 557KJ/mol | C. | 221.6KJ/mol | D. | 436KJ/mol |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com