
分析 (1)碘和碘離子反應生成I3-,碘在四氯化碳中呈紫色,I3-呈無色;
(2)NaCl和硝酸銀反應生成AgCl白色沉淀,AgCl和反應生成絡合物Ag(NH3)2Cl;
(3)Fe3+和SCN-反應生成絡合物而使溶液呈血紅色;
(4)硫酸銅和一水合氨發生復分解反應生成Cu(OH)2藍色沉淀,Cu(OH)2和一水合氨反應生成絡合物[Cu(NH3)4]2+,得到透明深藍色溶液,[Cu(NH3)4]SO4在乙醇中的溶解度小于在水中的溶解度,向溶液中加入乙醇后會析出深藍色晶體[Cu(NH3)4]SO4.
解答 解:(1)碘在四氯化碳中呈紫色,碘和碘離子發生氧化還原反應生成I3-,I3-呈無色,所以看到的現象是:溶液紫色變淺,離子反應方程式為I2+I-=I3-,故答案為:紫色變淺;I2+I-=I3-;
(2)NaCl和硝酸銀反應生成AgCl白色沉淀,AgCl和反應生成絡合物Ag(NH3)2Cl,沉淀溶解方程式為AgCl+2NH3.H2O=Ag(NH3)2Cl+2H2O,
故答案為:AgCl+2NH3.H2O=Ag(NH3)2Cl+2H2O;
(3)Fe3+和SCN-反應生成絡合物而使溶液呈血紅色,看到的現象是溶液變為血紅色,離子方程式為Fe3++3SCN-=Fe(SCN)3 ,
故答案為:溶液變為血紅色;Fe3++3SCN-=Fe(SCN)3 ;
(4)硫酸銅和一水合氨發生復分解反應生成Cu(OH)2藍色沉淀,離子反應方程式為Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+,Cu(OH)2和一水合氨反應生成絡合物[Cu(NH3)4]2+,得到透明藍色溶液,離子方程式為Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-,[Cu(NH3)4]SO4在乙醇中的溶解度小于在水中的溶解度,向溶液中加入乙醇后會析出深藍色晶體[Cu(NH3)4]SO4,
故答案為:深藍色;Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-;深藍色.
點評 本題考查配合物的有關化學方程式、離子方程式,明確物質的性質及物質之間的反應是解本題關鍵,知道鐵離子的檢驗方法及實驗現象,難點是配合物離子方程式的書寫.


科目:高中化學 來源: 題型:選擇題
| [H2]/mol•L-1 | [Cl2]/mol•L-1 | v/mol•L-1•s-1 |
| 1.0 | 1.0 | 1.0k |
| 2.0 | 1.0 | 2.0k |
| 2.0 | 4.0 | 4.0k |
| A. | m=1、n=1 | B. | m=$\frac{1}{2}$、n=$\frac{1}{2}$ | C. | m=$\frac{1}{2}$、n=1 | D. | m=1、n=$\frac{1}{2}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
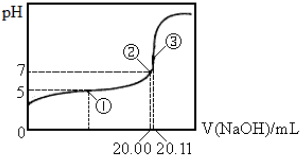
| A. | 該溫度下CH3COOH的電離平衡常數約為1.8×10-5 | |
| B. | 點①處溶液中c(CH3COO-)<c(CH3COOH) | |
| C. | 點③處溶液中c(OH-)=c(CH3COOH)+c(H+) | |
| D. | 滴定過程中不可能出現:c(CH3COOH)>c(CH3COO-)>c(OH-)>c(Na+)>c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
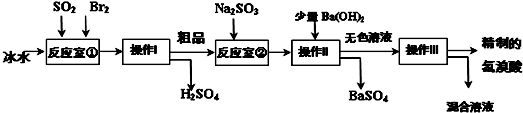
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 (1)拆開1mol H-H鍵、1mol N-H鍵、1mol N=N鍵分別需要吸收的能量為436KJ,391KJ,946KJ,求:則①1molN2生成NH3需要放出(吸收或放出)熱量92KJ;
(1)拆開1mol H-H鍵、1mol N-H鍵、1mol N=N鍵分別需要吸收的能量為436KJ,391KJ,946KJ,求:則①1molN2生成NH3需要放出(吸收或放出)熱量92KJ;查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 達到平衡時X濃度為0.04 mol•L-1 | |
| B. | 將容器體積變為20 L,Z的平衡濃度變為0.015 mol•L-1 | |
| C. | 若升高溫度,X的體積分數增大,則該反應的?△H<0 | |
| D. | 若增大壓強,平衡向正反應方向移動,平衡常數變大 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
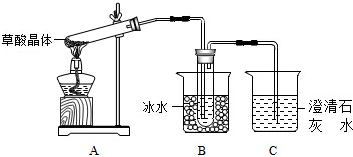

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com