
分析 設的N2 和H2的物質的量分別為xmol、ymol,則$\frac{28x+2y}{x+y}$=4.25×2,整理可得x:y=1:3,假設N2 和H2的物質的量分別為1mol、3mol,達到平衡時,NH3占25%,則:
N2(g)+3H2(g)?2NH3(g)
起始(mol):1 3 0
轉化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
所以$\frac{2x}{4-2x}$=25%,解得x=0.4
(1)相同條件下,氣體體積之比等于其物質的量之比;
(2)轉化率=$\frac{物質的量變化量}{起始物質的量}$×100%;
(3)混合氣體總質量不變,容器容積不變,混合氣體密度不變;
(4)恒溫恒容下,壓強之比等于氣體物質的量之比.
解答 解:設的N2 和H2的物質的量分別為xmol、ymol,則$\frac{28x+2y}{x+y}$=4.25×2,整理可得x:y=1:3,假設N2 和H2的物質的量分別為1mol、3mol,達到平衡時,NH3占25%,則:
N2(g)+3H2(g)?2NH3(g)
起始(mol):1 3 0
轉化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
所以$\frac{2x}{4-2x}$=25%,解得x=0.4
(1)相同條件下,氣體體積之比等于其物質的量之比,故進入容器N2和H2的 體積比為1mol:3mol=1:3,故答案為:1:3;
(2)氮氣轉化率=$\frac{0.4mol}{1mol}$×100%=40%,故答案為:40%;
(3)混合氣體總質量不變,容器容積不變,混合氣體密度不變,即反應前后的密度比為1:1,故答案為:1:1;
(4)恒溫恒容下,壓強之比等于氣體物質的量之比,故反應前后的壓強比為(1+3)mol:(4-0.8)mol=5:4,故答案為:5:4.
點評 本題考查化學平衡計算,關鍵是計算氮氣與氫氣起始物質的量之比,注意利用賦值法解答,注意三段式解題法在化學平衡計算中應用.


 智慧小復習系列答案
智慧小復習系列答案科目:高中化學 來源: 題型:解答題
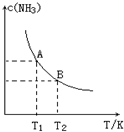 將1mol N2(g)和3mol H2(g)通入一個10L的恒容密閉容器中發生反應,在不同溫度下達到平衡時NH3(g)的平衡濃度如圖所示.其中溫度為T1時平衡混合氣體中氨氣的體積分數為25%,反應中放出a kJ熱量.
將1mol N2(g)和3mol H2(g)通入一個10L的恒容密閉容器中發生反應,在不同溫度下達到平衡時NH3(g)的平衡濃度如圖所示.其中溫度為T1時平衡混合氣體中氨氣的體積分數為25%,反應中放出a kJ熱量.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ②③ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 達到化學平衡時,N2將完全轉化為NH3 | |
| B. | 達到化學平衡時,N2、H2和NH3的物質的量濃度一定相等 | |
| C. | 達到化學平衡時,正反應和逆反應的速率都為零 | |
| D. | 達到化學平衡時,N2和H2的轉化率相同且c(N2):c(H2)=1:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 實驗室制備1,2-二溴乙烷的反應原理如下:
實驗室制備1,2-二溴乙烷的反應原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 狀態 | 無色液體 | 無色液體 | 無色液體 |
| 密度g/cm3 | 0.79 | 2.2 | 0.71 |
| 沸點/℃ | 78.5 | 132 | 34.6 |
| 熔點/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 短周期元素X.Y.Z.W在元素周期表中的相對位置如圖所示,其中w原子的最外層電子數是最內層電子數的3倍.下列判斷不正確的是( )
短周期元素X.Y.Z.W在元素周期表中的相對位置如圖所示,其中w原子的最外層電子數是最內層電子數的3倍.下列判斷不正確的是( )| A. | x與同主族且相鄰元素的氣態氫化物的沸點,前者高于后者 | |
| B. | 含Y元素的鹽溶液有的顯酸性,有的顯堿性 | |
| C. | x的氣態氫化物與w的最高價氧化物的水化物反應只能生成一種鹽 | |
| D. | x與H、O元素形成的化合物可以組成一種鹽,其中X.H.O元素原子個數之比為2:4:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鈉和鉀的合金可用于快中子反應堆作熱交換劑 | |
| B. | 可用超純硅制造的單晶硅來制芯片 | |
| C. | 可利用二氧化碳制造全降解塑料 | |
| D. | 氯氣有毒,不能用于藥物的合成 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com