
 食鹽中的抗結劑是亞鐵氰化鉀,其化學式為K4[Fe(CN)6]•3H2O.42.2g K4[Fe(CN)6]•3H2O,樣品受熱脫水過程的熱重曲線(樣品質量隨溫度的變化曲線)如圖所示.(已知K4[Fe(CN)6]•3H2O相對分子質量為422;K4[Fe(CN)6]相對分子質量為368)
食鹽中的抗結劑是亞鐵氰化鉀,其化學式為K4[Fe(CN)6]•3H2O.42.2g K4[Fe(CN)6]•3H2O,樣品受熱脫水過程的熱重曲線(樣品質量隨溫度的變化曲線)如圖所示.(已知K4[Fe(CN)6]•3H2O相對分子質量為422;K4[Fe(CN)6]相對分子質量為368)分析 (1)42.2g K4[Fe(CN)6]•3H2O的物質的量為0.1mol,含有結晶水質量為0.1mol×3×18g/mol=5.4g,而150℃時固體物質的質量為36.8g,質量減少為42.2g-36.8g=5.4g,故150℃完全失去結晶水;
(2)亞鐵氰化鉀水溶液與酸反應放出極毒的氰化氫(HCN)氣體,加熱至一定溫度時能分解產生氰化鉀(KCN),由圖可知應在400℃,故應避免與酸性物質物質一起烹飪、控制烹飪溫度不超過400℃;
(3)發生反應:KCN+HCl═KCl+HCN,若是等濃度,生成HCN應該呈酸性,而反應后PH=7呈中性,說明KCN有剩余(KCN水解呈堿性);
HCN?H++CN-的電離平衡常數Ka=$\frac{c({H}^{+})×c(C{N}^{-})}{c(HCN)}$,溶液呈中性,則c(H+)=c(OH-)=10-7 mol/L,由電荷守恒c(H+)+c(K+)=c(CN-)+c(Cl-)+c(OH-),故c(K+)=c(CN-)+c(Cl-),則c(CN-)=(0.5a-0.005)mol/L,根據物料守恒c(HCN)=0.5amol/L-c(CN-)=0.005mol/L,代入電離平衡常數表達式計算;
(4)催化劑的特點,恢復原來狀態,則Fe3+→Fe2+,故Fe3+將SO2氧化為硫酸;可以降低SO2的污染,同時制得硫酸;
(5)根據c(Fe3+)=$\frac{Ksp}{{c}^{3}(O{H}^{-})}$計算判斷.
解答 解:(1)42.2g K4[Fe(CN)6]•3H2O的物質的量為0.1mol,含有結晶水質量為0.1mol×3×18g/mol=5.4g,而150℃時固體物質的質量為36.8g,質量減少為42.2g-36.8g=5.4g,故150℃完全失去結晶水,則150℃時固體物質的化學式為:K4[Fe(CN)6],
故答案為:K4[Fe(CN)6];
(2)亞鐵氰化鉀水溶液與酸反應放出極毒的氰化氫(HCN)氣體,加熱至一定溫度時能分解產生氰化鉀(KCN),由圖可知應在400℃,故應避免避免與醋等酸性物質一起烹飪、控制烹飪溫度不超過400℃,
故答案為:避免與醋等酸性物質一起烹飪;控制烹飪溫度不超過400℃;
(3)發生反應:KCN+HCl═KCl+HCN,若是等濃度,生成HCN應該呈酸性,而反應后PH=7呈中性,說明KCN有剩余(KCN水解呈堿性),所以a>0.01mol/L;
HCN?H++CN-的電離平衡常數Ka=$\frac{c({H}^{+})×c(C{N}^{-})}{c(HCN)}$,溶液呈中性,則c(H+)=c(OH-)=10-7 mol/L,由電荷守恒c(H+)+c(K+)=c(CN-)+c(Cl-)+c(OH-),故c(K+)=c(CN-)+c(Cl-),則c(CN-)=(0.5a-0.005)mol/L,根據物料守恒c(HCN)=0.5amol/L-c(CN-)=0.005mol/L,則Ka=$\frac{c({H}^{+})×c(C{N}^{-})}{c(HCN)}$=$\frac{1{0}^{-7}×(0.5a-0.005)}{0.005}$mol•L-1 =(100a-1)×10-7 mol•L-1
故答案為:>;(100a-1)×10-7 mol•L-1;
(4)催化劑的特點,恢復原來狀態,則Fe3+→Fe2+,故Fe3+將SO2氧化為硫酸,反應離子方程式為:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,上述轉化的重要意義在于:可以消除SO2的污染,同時制得硫酸,變廢為寶,
故答案為:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;以消除SO2的污染,同時制得硫酸,變廢為寶;
(5)c(Fe3+)=$\frac{Ksp}{{c}^{3}(O{H}^{-})}$=1.1×10-3 mol•L-1>1×10-5 mol•L-1,故Fe3+沒有沉淀完全,
故答案為:c(Fe3+)=$\frac{Ksp}{{c}^{3}(O{H}^{-})}$=1.1×10-3 mol•L-1>1×10-5 mol•L-1,故Fe3+沒有沉淀完全.
點評 本題考查化學方程式計算、弱電解質電離、溶度積有關計算等,是對學生綜合能力的考查,需要學生具備扎實的基礎,難度中等.


 奪冠訓練單元期末沖刺100分系列答案
奪冠訓練單元期末沖刺100分系列答案科目:高中化學 來源: 題型:選擇題
| A. | 1:1 | B. | 15:13 | C. | 7:8 | D. | 8:7 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 常溫常壓下測得1 mol N2的質量為28 g | |
| B. | 用量筒測得排水法收集到的氫氣體積為50.28 mL | |
| C. | 用兩只250 mL的容量瓶配制0.1 mol/L 500 mL的NaOH溶液 | |
| D. | 用托盤天平稱得2.5 g膽礬,受熱充分失水后,固體質量減輕0.9 g |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 2CH3CHO+2H2O
2CH3CHO+2H2O 
 (其中一種)
(其中一種)查看答案和解析>>
科目:高中化學 來源: 題型:解答題
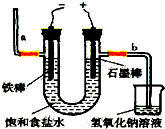 氯氣是一種重要的化工原料,自來水消毒、農藥的生產、藥物的合成等都需要用到氯氣.工業上通常采用電解法制氯氣:觀察如圖,回答:
氯氣是一種重要的化工原料,自來水消毒、農藥的生產、藥物的合成等都需要用到氯氣.工業上通常采用電解法制氯氣:觀察如圖,回答:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度(℃) | 450 | 500 | 550 | 600 |
| SO2的轉化率(%) | 97.5 | 95.8 | 90.50 | 80.0 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com