
| A. | H2SO4的酸性比HClO的酸性強,所以S的非金屬性比Cl強 | |
| B. | Mg(OH)2是中強堿,Al(OH)3是兩性氫氧化物,所以Al比Mg活潑 | |
| C. | H2S 300℃時開始分解,H2O 1000℃時開始分解,說明O的非金屬性比S強 | |
| D. | Na和Mg與酸都能激烈反應放出氫氣,故無法比較它們的金屬性強弱 |
分析 A.非金屬元素最高價氧化物的水化物酸性越強,其非金屬性越強;
B.金屬元素最高價氧化物的水化物堿性越強,其金屬性越強;
C.元素的非金屬性越強,其氫化物的穩定性越強;
D.金屬元素的金屬性越強,金屬與相同濃度的同一種酸反應越劇烈.
解答 解:A.非金屬元素最高價氧化物的水化物酸性越強,其非金屬性越強,HClO不是Cl元素的最高價含氧酸,所以不能根據硫酸和次氯酸酸性強弱判斷非金屬性強弱,故A錯誤;
B.金屬元素最高價氧化物的水化物堿性越強,其金屬性越強,Mg(OH)2是中強堿,Al(OH)3是兩性氫氧化物,所以Mg比Al活潑,故B錯誤;
C.元素的非金屬性越強,其氫化物的穩定性越強,H2S 300℃時開始分解,H2O 1000℃時開始分解,說明O的非金屬性比S強,故C正確;
D.金屬元素的金屬性越強,金屬與相同濃度的同一種酸反應越劇烈,Na和Mg與酸都能激烈反應放出氫氣,但劇烈程度不同,所以可以比較金屬性強弱,故D錯誤;
故選C.
點評 本題考查金屬性、非金屬性強弱判斷,為高頻考點,明確金屬性、非金屬性強弱判斷方法即可解答,易錯選項是A,題目難度不大.


 第1卷單元月考期中期末系列答案
第1卷單元月考期中期末系列答案科目:高中化學 來源: 題型:選擇題
| A. | 通入溴水中觀察溶液顏色的變化 | B. | 嗅聞它們的氣味 | ||
| C. | 比較它們在水中的溶解度大小 | D. | 點燃它們后,觀察火焰 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
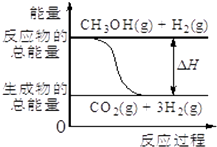 已知CH3OH(g)+H2O(g)=CO2(g)+3H2(g),該反應中的能量變化如圖所示下列說法不正確的是( )
已知CH3OH(g)+H2O(g)=CO2(g)+3H2(g),該反應中的能量變化如圖所示下列說法不正確的是( )| A. | 該反應拆開反應物所有鍵所吸收的總能量小于形成生成物所放出的總能量 | |
| B. | 該反應是放熱反應 | |
| C. | 該反應不能設計成原電池 | |
| D. | 該反應所有分子中各原子都以共價鍵相結合? |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③ | B. | ①② | C. | ②③ | D. | 全部 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{a}{A}$(A-Z+m)mol | B. | $\frac{a}{A}$(A-Z)mol | C. | $\frac{a}{A+m}$(A-Z)mol | D. | $\frac{a}{A+m}$(A-Z+m)mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com