
| 物質 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |

| Kw[Fe(OH)3] |
| C3(OH-) |
| Kw[Fe(OH)3] |
| C3(OH-) |
| 2.6×10-39 |
| (1×10-10)3 |
| 0.002mol×171g/mol |
| 0.36g |


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
| A、金屬鎂與稀鹽酸反應:有氣泡逸出:Mg+2H++2Cl-═MgCl2+H2↑ |
| B、NaHCO3溶液中加入過量的Ba(OH)2溶液:有白色沉淀產生2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32- |
| C、碳酸鈉溶液與鹽酸反應:有氣泡逸出:Na2CO3+2H+═2Na++CO2↑+H2O |
| D、氯化鋇溶液與稀硫酸反應:有白色沉淀生成:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、飲用酸性飲料 |
| B、在牙膏中添加適量的Ca2+離子 |
| C、少吃甜食 |
| D、在牙膏中加入氟化物添加劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、可以根據PbI2和AgCl的Ksp的大小比較兩者的溶解度 |
| B、常溫下,同濃度的Na2S與NaHS溶液相比,NaHS溶液的pH大 |
| C、等物質的量濃度的CH3COONH4溶液和NH4HSO4溶液,前者的c(NH4+)小 |
| D、用惰性電極電解飽和NaCl溶液,若有1.0 mol電子轉移,則理論生成1.0 mol NaOH |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、向AgCl飽和溶液中加入NaCl固體,AgCl的Ksp增大 |
| B、AgCl不溶于水,溶液中沒有Cl-和Ag+ |
| C、AgCl沉淀的生成和溶解仍在不斷進行,但速率相等 |
| D、向AgCl飽和溶液中加入NaCl固體,沒有AgCl產生 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 在調水工程中,沿途工業污水的任意排放是造成水質惡化的最大隱患.檢測某工廠廢液中含有大量Mg2+、Al3+、Fe3+、Ag+、Ba2+等離子.試分析回答下列問題:
在調水工程中,沿途工業污水的任意排放是造成水質惡化的最大隱患.檢測某工廠廢液中含有大量Mg2+、Al3+、Fe3+、Ag+、Ba2+等離子.試分析回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
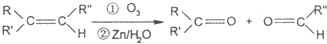
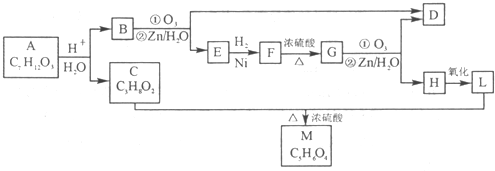
查看答案和解析>>
科目:高中化學 來源: 題型:
| 物質的量 | 0(min) | 10(min) | 20(min) | 30(min) | 40(min) | 50(min) | 60(min) |
| NO | 1 | 0.8 | 0.58 | 0.4 | 0.4 | 0.32 | 0.32 |
| N2 | 0 | 0.1 | 0.21 | 0.3 | 0.3 | 0.34 | 0.34 |
| CO2 | 0 | 0.1 | 0.21 | 0.3 | 0.3 | 0.17 | 0.17 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com