
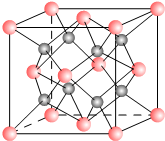
 一種離子晶體的晶胞如右圖.其中陽離子A以
一種離子晶體的晶胞如右圖.其中陽離子A以分析 (1)利用均攤法計算離子數目;
(2)根據離子的化合價及與其電子層結構相同的惰性氣體元素判斷該離子元素,從而寫出其化學式;
(3)陽離子周圍距離最近的陰離子數為8,陰離子周圍距離最近的陽離子數是4;
(4)根據A離子的半徑金屬晶胞的邊長,再利用體積公式計算.
解答 解:(1)每個晶胞中含A離子的數目=8×$\frac{1}{8}$=4,含B離子數目為8,
故答案為:4;8;
(2)通過(1)知,該物質的化學式為:AB2,A是金屬陽離子,則A的化合價是+2價,若A的核外電子排布與Ar相同,則A是Ca元素,B的化合價是-1價,且B的電子排布與Ne相同,則B是F元素,則該離子化合物的化學式是CaF2,
故答案為:CaF2;
(3)陽離子周圍距離最近的陰離子數為8,陰離子周圍距離最近的陽離子數是4,
故答案為:8;4;
(4)該晶胞中正方形對角線的長度=4rm,則該晶胞的邊長=2$\sqrt{2}$rm,則該晶胞的體積=(2$\sqrt{2}$rm)3=16$\sqrt{2}$r3 m3,
故答案為:16$\sqrt{2}$r3 .
點評 本題考查了晶胞的有關計算,難點是配位數、晶胞體積的計算,注意晶胞邊長不等于A離子直徑,為易錯點.


科目:高中化學 來源: 題型:解答題
 某些廢舊塑料可采用下列方法處理,將廢塑料隔絕空氣加強熱,使其變成有用的物質,實驗裝置如圖.
某些廢舊塑料可采用下列方法處理,將廢塑料隔絕空氣加強熱,使其變成有用的物質,實驗裝置如圖.| 產物 | 氫氣 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 質量分數(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
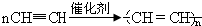 .
.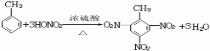 ;該物質的一氯代物有4種.
;該物質的一氯代物有4種.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 組別 | 陽極 | 陰極 | 甲溶液 | 物質乙 |
| A | Ag | Cu | AgNO3溶液 | AgNO3固體 |
| B | C | Cu | CuSO4溶液 | Cu(OH)2 |
| C | Pt | Pt | NaOH溶液 | NaOH固體 |
| D | C | Fe | NaCl溶液 | HCl |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 (I)由短周期元素構成的A~E五種物質中都含有同一種元素,B為單質.
(I)由短周期元素構成的A~E五種物質中都含有同一種元素,B為單質.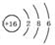 ,A既能與強酸又能與強堿反應,且都能產生氣體,請畫出A的電子式為
,A既能與強酸又能與強堿反應,且都能產生氣體,請畫出A的電子式為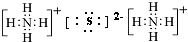 或
或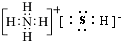 .
.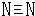
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
 有A、B、C、D、E、F六種短周期元素,其元素特征信息如表:
有A、B、C、D、E、F六種短周期元素,其元素特征信息如表:| 元素編號 | 元素特征信息 |
| A | A的單質是密度最小的物質 |
| B | B的單質能與冷水劇烈反應,所得強堿性溶液中含有兩種電子數相同的陰、陽離子 |
| C | C的原子最外層電子數是其內層電子數的三倍 |
| D | D與B同周期,該周期中D的簡單離子半徑最小 |
| E | B、C、E組成的36電子的化合物Y是家用消毒劑的主要成分 |
| F | F元素最高正價與最低負價的代數和為4 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 食用白糖的主要成分是蔗糖 | |
| B. | 油脂、淀粉和蛋白質都是高分子化合物 | |
| C. | 油脂不能使溴水褪色 | |
| D. | 乙酸乙酯和食用油都可以水解生成乙醇 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com