
| 實驗序號 | 實驗步驟和操作 | 實驗現象 |
| 實驗一 | (Ⅰ)取氯化亞鐵固體[已部分變質,含有少量難溶于水的雜質Fe(OH)2Cl],向其中加入過量稀鹽酸. (Ⅱ)再加入稍過量的鐵粉,振蕩. | 固體完全溶解,溶液呈黃綠色 Fe(OH)2Cl+2H+=Fe3++Cl-+2H2O |
| 實驗二 | (Ⅰ)取實驗一得到的溶液,加入KSCN溶液. (Ⅱ)再加入少量H2O2溶液. | 顏色無明顯變化 溶液變紅,有少量氣泡 |
| 實驗三 | (Ⅰ)取10mL 0.1mol/L KI溶液,滴加6滴0.1mol/L FeCl3溶液. (Ⅱ)取少量上述黃色溶液,滴加KSCN溶液. (Ⅲ)另取上述的黃色溶液,加入淀粉溶液. | 溶液呈黃色 溶液變紅 溶液變藍 |
| 實驗四 | (Ⅰ)向實驗三步驟I中所得的黃色溶液中加入2mL CCl4,充分振蕩后,分離得到水層;重復操作三次. (Ⅱ)向步驟I中所得水層中加入KSCN溶液. | 顏色無明顯變化 |
分析 (1)Fe(OH)2Cl與鹽酸反應生成氯化鐵和水;
(2)實驗一步驟(II)中Fe與鹽酸、鐵離子反應均生成亞鐵離子;
(3)實驗二步驟(II)中亞鐵離子被H2O2氧化;
(4)實驗三步驟(I)中KI與FeCl3發生氧化還原反應生成碘化亞鐵、碘、KCl;
(5)已知用KSCN檢驗Fe3+時,Fe3+的最低顯色濃度為1×10-3mol/L,實驗四中最終溶液不變紅,與鐵離子濃度低有關.
解答 解:(1)實驗一步驟(I)中Fe(OH)2Cl與鹽酸反應的離子方程式是Fe(OH)2Cl+2H+=Fe3++Cl-+2H2O,故答案為:Fe(OH)2Cl+2H+=Fe3++Cl-+2H2O;
(2)實驗一步驟(II)中發生Fe+2H+=Fe2++H2↑、2Fe3++Fe=3Fe2+,觀察到的實驗現象是溶液變為淺綠色,且有無色氣體生成;加入稍過量鐵粉的作用是防止亞鐵離子被氧化為鐵離子,故答案為:溶液變為淺綠色,且有無色氣體生成;防止亞鐵離子被氧化為鐵離子;
(3)實驗二步驟(II)中溶液變紅的原因是2H++2Fe2++H2O2=2Fe3++2H2O、Fe3++3SCN-=Fe(SCN)3,
故答案為:2H++2Fe2++H2O2=2Fe3++2H2O、Fe3++3SCN-=Fe(SCN)3;
(4)實驗三步驟(I)中KI與FeCl3發生氧化還原反應生成碘化亞鐵、碘、KCl,離子反應為2Fe3++2I-?2Fe2++I2,可知實驗三步驟(I)中的黃色液體中含有的溶質微粒除了K+、Cl-,還有Fe3+、I-、Fe2+、I2,故答案為:Fe3+、I-、Fe2+、I2;
(5)已知用KSCN檢驗Fe3+時,Fe3+的最低顯色濃度為1×10-3mol/L.實驗四中最終溶液不變紅的原因是碘被萃取至CCl4中,水層中的c(I2) 下降,平衡2Fe3++2I-?2Fe2++I2正向移動,多次萃取后,Fe3+的濃度下降至1×10-3mol/L以下,無法顯色,故答案為:碘被萃取至CCl4中,水層中的c(I2) 下降,平衡2Fe3++2I-?2Fe2++I2正向移動,多次萃取后,Fe3+的濃度下降至1×10-3mol/L以下,無法顯色.
點評 本題考查性質實驗方案的設計,為高頻考點,把握鐵三角的轉化及實驗中發生的反應、現象為解答的關鍵,注意側重分析與實驗能力的考查,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 常溫時,等濃度的溶液的堿性:Na2CO3<NaHCO3 | |
| B. | 二者均可與澄清石灰水反應生成白色沉淀 | |
| C. | 與同濃度的鹽酸反應放出氣體的速率快慢:Na2CO3>NaHCO3 | |
| D. | 等質量的Na2CO3和NaHCO3分別與過量的鹽酸反應,產物CO2的質量相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二氧化硅熔點高硬度大,可用于制作光導纖維 | |
| B. | 氫氧化鋁具有弱堿性,可用于胃酸中和劑 | |
| C. | 鐵比銅活潑,氯化鐵不能用于腐蝕銅板 | |
| D. | 氧化鐵能與酸反應,可用于制作紅色涂料 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 短周期元素T、Q、R、W、Z在元素周期表中的位置如右圖所示,其中T所處的周期序數與主族序數相等,請回答下列問題:
短周期元素T、Q、R、W、Z在元素周期表中的位置如右圖所示,其中T所處的周期序數與主族序數相等,請回答下列問題: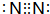
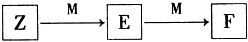
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
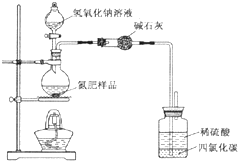 某氮肥硫酸銨中混有硫酸氫銨.為測定該氮肥的含氮量,一化學研究性學習小組取一定量氮肥樣品,研磨使其混合均勻,備用.已知:
某氮肥硫酸銨中混有硫酸氫銨.為測定該氮肥的含氮量,一化學研究性學習小組取一定量氮肥樣品,研磨使其混合均勻,備用.已知:| 氫氧化鈉溶液體積/mL | 40.00mL | ||
樣品質量/g | 7.750 | 15.50 | 23.25 |
氨氣質量/g | 1.870 | 1.870 | 1.700 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 砂濾是利用過濾原理除去水中較大的固體顆粒 | |
| B. | 臭氧可以消毒殺菌是因為臭氧有強氧化性 | |
| C. | 游泳池水中的臭氧濃度越大越好 | |
| D. | 活性炭可以吸附水中懸浮的雜質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②③ | B. | ②③④ | C. | ①②③⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
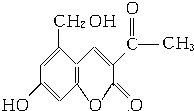 它配以輔料丙二醇溶成針劑用于臨床.假藥中使用廉價的二甘醇作為輔料,二甘醇為工業溶劑,有很強的毒性.請回答下列問題:
它配以輔料丙二醇溶成針劑用于臨床.假藥中使用廉價的二甘醇作為輔料,二甘醇為工業溶劑,有很強的毒性.請回答下列問題: .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com