
時間(h) 物質的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | 1.00 | 1.00 |
分析 (1)根據化學平衡狀態的特征解答,當反應達到平衡狀態時,正逆反應速率相等,各物質的濃度、百分含量不變,以及由此衍生的一些量也不發生變化,解題時要注意,選擇判斷的物理量,隨著反應的進行發生變化,當該物理量由變化到定值時,說明可逆反應到達平衡狀態;
(2)①依據反應的焓變結合化學方程式計算放出的熱量;
②根據氨氣的物質的量計算出消耗的氮氣的物質的量,再根據v=$\frac{△c}{△t}$計算出0~1小時內N2的平均反應速度率;
③根據3、4小時的時間段氨氣的物質的量不變,說明達到了平衡狀態,根據氨氣的物質的量計算出消耗的氮氣和氫氣的物質的量及平衡時的濃度,
再根據平衡常數表達式K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$計算出該溫度下的平衡常數;
④根據加入氨氣、水和氨氣后的濃度商判斷平衡移動方向.
解答 解:(1)a.單位時間內生成2n mol NH3的同時生成3n mol H2,說明正逆反應速率相等,達到了平衡狀態,故a正確;
b.若達到平衡狀態時,單位時間內生成6n mol N-H鍵的同時會生成3n mol H-H鍵,說明此時沒有達到平衡狀態,故b錯誤;
c.用N2、H2、NH3的物質的量濃度變化表示的反應速率之比為1:3:2,與是否達到平衡狀態無關,故c錯誤;
d.混合氣體的平均摩爾質量不變,說明總物質的量不變,正逆反應速率相等,達到化學平衡狀態,故d正確;
e.混合氣體的密度不變,反應發生到平衡這個量一直不變,故e錯誤;
f.隨反應進行,混合氣體物質的量變化,容器內壓強發生變化,壓強保持不變說明到達平衡,故f正確;
故答案為:adf;
(2)①N2(g)+3H2(g)?2NH3(g)△H=-92.20kJ•mol-1,生成2mol氨氣放熱92.30kJ,反應進行到2小時時,氮氣的物質的量變化了1.5mol-1.2mol=0.3mol,則生成氨氣0.6mol,放出的熱量為$\frac{92.60}{2}$kJ/mol×0.6mol=27.78kJ,
故答案為:27.78;
②0~1小時內生成了0.2mol氨氣,根據反應N2(g)+3H2(g)?2NH3(g),消耗了氮氣的物質的量為:n(N2)=$\frac{1}{2}$n(NH3)=0.1mol,0~1小時內N2的平均反應速度率為:v(N2)=$\frac{\frac{0.1mol}{2L}}{1h}$=0.05mol/(L•h),
故答案為:0.05;
③根據表中數據可知,反應在第3和4小時時間段內氨氣的物質的量不變,說明達到了平衡狀態,此時生成了1.00mol氨氣,
列出化學平衡的三段式為 N2(g)+3H2(g)?2NH3(g),
反應開始前(mol) 1.5 4.5 0
變化量(mol) 0.5 1.5 1
平衡時(mol) 1 3 1
平衡時濃度(mol/L) 0.500 1.500 0.5
此溫度下該反應的化學平衡常數K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$=$\frac{0.{5}^{2}}{1.{5}^{3}×0.5}$≈0.15,
故答案為:0.15;
④反應達到平衡后,若往平衡體系中再加入N2、H2O、NH3各1mol,此時各組分的濃度為:
c(N2)=$\frac{1.00mol+1.00mol}{2L}$=1.00mol/L,c(H2)=$\frac{3.00mol+1.00mol}{2L}$=2.00mol/L,c(N2)=$\frac{1.00mol+1.00mol}{2L}$=1.00mol/L,
濃度商為:$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$=$\frac{{1}^{2}}{{2}^{3}×1}$=0.125<k=0.15,所以平衡向著正向移動,
故答案為:正反應.
點評 本題考查了化學平衡狀態的判斷、反應熱的計算、化學平衡常數的計算與應用、化學反應速率與化學計量數的關系等知識,涉及的知識點較多,試題綜合性強,難度較大,有利于培養學生的邏輯思維能力和發散思維能力,提高學生的應試能力和學習效率.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 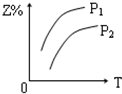 | B. | 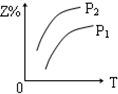 | C. | 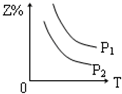 | D. | 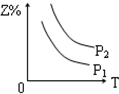 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 與鋁產生氫氣的溶液中:NH4+、Cl-、Mg2+、SO42- | |
| B. | 常溫下PH=9的溶液中:Na+、K+、AlO2-、SO42- | |
| C. | 0.1mol/LNaOH溶液中:HCO3-、Na+、K+、Ca2+ | |
| D. | 無色溶液中:H+、Cu2+、Al3+、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2H2(g)+O2(g)═2H2O(g)△H1 2H2(g)+O2(g)═2H2O(l)△H2 | |
| B. | S(s)+O2(g)═SO2(g)△H1 S(g)+O2(g)═SO2(g)△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1 C(s)+O2(g)═CO2(g)△H2 | |
| D. | H2(g)+Cl2(g)═2HCl(g)△H1 $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用食醋清除暖水瓶中的水垢 | |
| B. | 纖維素在人體內可水解為葡萄糖,故可作為人類的營養物質 | |
| C. | 用熱的純堿水洗滌油垢 | |
| D. | 葡萄糖中花青素在堿性環境下顯紫色,故可用蘇打粉打粉檢驗假紅酒 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com