
【題目】磷元素在生產和生活中有廣泛的應用
(1)P原子價電子排布圖為_________。
(2)四(三苯基膦)鈀分子結構如下圖1:

P原子以正四面體的形態圍繞在鈀原子中心上,鈀原子的雜化軌道類型為_________;判斷該物質在水中溶解度并加以解釋_________,該物質可用于圖2所示物質A的合成:
物質A中碳原子雜化軌道類型為 _________;一個A分子中手性碳原子數目為 _________。
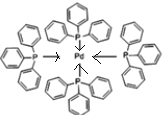
(3)在圖3中表示出四(三苯基膦)鈀分子中配位鍵:
(4)PCl5是一種白色晶體,在恒容密閉容器中加熱可在148℃液化,形成一種能導電的熔體,測得其中含有一種正四面體形陽離子和一種正六面體形陰離子,熔體中P-Cl的鍵長只有198nm和206nm兩種,這兩種離子的化學式為_________;正四面體形陽離子中鍵角小于PCl3的鍵角原因為_________;該晶體的晶胞如右圖4所示,立方體的晶胞邊長為apm,NA為阿伏伽德羅常數的值,則該晶體的密度為_________g/cm3.
(5)PBr5氣態分子的結構與PCl5相似,它的熔體也能導電,經測定知其中只存在一種P-Br鍵長,試用電離方程式解釋PBr5熔體能導電的原因_________。
【答案】(1)![]() ;(2)sp3;不易溶于水,水為極性分子,四(三苯基膦)鈀分子為非極性分子,分子極性不相似,故不相溶;sp、sp2、sp3;3;
;(2)sp3;不易溶于水,水為極性分子,四(三苯基膦)鈀分子為非極性分子,分子極性不相似,故不相溶;sp、sp2、sp3;3;
(3) ;(4)PCl4+和PCl6-;兩分子中P原子雜化方式均為sp3雜化,PCl3分子中P原子有一對孤電子對,PCl4+中P沒有孤電子對.孤電子對對成鍵電子的排斥力大于成鍵電子對間的排斥力;
;(4)PCl4+和PCl6-;兩分子中P原子雜化方式均為sp3雜化,PCl3分子中P原子有一對孤電子對,PCl4+中P沒有孤電子對.孤電子對對成鍵電子的排斥力大于成鍵電子對間的排斥力;![]() ;(5)PBr5=PBr4++Br-
;(5)PBr5=PBr4++Br-
【解析】
試題分析:(1)磷是15號元素,其原子核外有15個電子,P元素基態原子電子排布為1s22s22p63s23P3,P的最外層3p電子3個電子自旋方向相同,為![]() ,故答案為:
,故答案為:![]() ;
;
(2)P原子以正四面體的形態圍繞在鈀原子中心上,鈀原子與P原子成4個單鍵,雜化軌道數為4,為sp3雜化,水為極性分子,四(三苯基膦)鈀分子為非極性分子,分子極性不相似,故不相溶,所以四(三苯基膦)鈀分子在水中難溶,物質A中甲基上的C采取sp3雜化類型,C≡N為SP雜化,碳碳雙鍵為sp2雜化,連接4個不同原子或原子團的碳原子為手性碳原子,如圖: ,所以一個A分子中手性碳原子數目為3個,故答案為:sp3;不易溶于水,水為極性分子,四(三苯基膦)鈀分子為非極性分子,分子極性不相似,故不相溶;sp、sp2、sp3;3;
,所以一個A分子中手性碳原子數目為3個,故答案為:sp3;不易溶于水,水為極性分子,四(三苯基膦)鈀分子為非極性分子,分子極性不相似,故不相溶;sp、sp2、sp3;3;
(3)配位鍵由含有孤電子對的原子指向含有空軌道的原子,Pd含有空軌道、P原子含有孤電子對,所以配位鍵由P原子指向Pd原子,如圖: ,故答案為:
,故答案為: ;
;
(4)PCl5是一種白色晶體,在恒容密閉容器中加熱可在148℃液化,形成一種能導電的熔體,說明生成自由移動的陰陽離子,一種正四面體形陽離子是PCl4+和一種正六面體形陰離子是PCl6-,即發生反應為:2PCl5=PCl4++PCl6-,PCl3中價層電子對個數=σ鍵個數+孤電子對個數=3+![]() =4,所以原子雜化方式是sp3,PCl5中價層電子對個數=σ鍵個數+孤電子對個數=5+
=4,所以原子雜化方式是sp3,PCl5中價層電子對個數=σ鍵個數+孤電子對個數=5+![]() (55×1)=4,所以原子雜化方式是sp3,PCl3分子中P原子有一對孤電子對,PCl4+中P沒有孤電子對.孤電子對對成鍵電子的排斥力大于成鍵電子對間的排斥力,所以PCl5中正四面體形陽離子中鍵角小于PCl3的鍵角,晶胞中PCl5位于頂點8×
(55×1)=4,所以原子雜化方式是sp3,PCl3分子中P原子有一對孤電子對,PCl4+中P沒有孤電子對.孤電子對對成鍵電子的排斥力大于成鍵電子對間的排斥力,所以PCl5中正四面體形陽離子中鍵角小于PCl3的鍵角,晶胞中PCl5位于頂點8×![]() =1,1個PCl5分子位于晶胞內部,立方體的晶胞邊長為a pm,所以密度為:ρ=
=1,1個PCl5分子位于晶胞內部,立方體的晶胞邊長為a pm,所以密度為:ρ=![]() =
=![]() ,故答案為:PCl4+
,故答案為:PCl4+![]() ;
;
(5)PBr5氣態分子的結構與PCl5相似,說明PBr5也能電離出能導電的陰陽離子,而產物中只存在一種P-Br鍵長,所以發生這樣電離PBr5═PBr4++Br-,故答案為:PBr5=PBr4++Br-。


科目:高中化學 來源: 題型:
【題目】硫代硫酸鈉是一種重要的化工產品。工業上常利用含硫廢水生產Na2S2O35H2O,實驗室可用如下裝置(略去部分加持儀器)模擬生成過程。


燒瓶C中發生反應如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (II)
S(s)+Na2SO3(aq)![]() Na2S2O3(aq) (III)
Na2S2O3(aq) (III)
(1)儀器組裝完成后,關閉兩端活塞,向裝置B中的長頸漏斗內注入液體至形成一段液注,若 ,則整個裝置氣密性良好。裝置D的作用是 。裝置E中為 溶液。
(2)為提高產品純度,應使燒瓶C中Na2S和Na2SO3恰好完全反應,則燒瓶C中Na2S和Na2SO3物質的量之比為 。
(3)裝置B的作用之一是觀察SO2的生成速率,其中的液體最好選擇 。
a.蒸餾水 b.飽和Na2SO3溶液
c.飽和NaHSO3溶液 d.飽和NaHCO3溶液
(4)實驗中,為使SO2緩慢進入燒瓶C,采用的操作是 。
(5)已知反應(III)相對較慢,則燒瓶C中反應達到終點的現象是 。
(6)反應終止后,燒瓶C中的溶液經蒸發濃縮冷卻,過濾,洗滌,干燥,即得到粗產品(主要含有Na2S2O35H2O和其他雜質)。某興趣小組為測定該產品純度,準確稱取4.96 g產品,用適量蒸餾水溶解,以淀粉作指示劑,用0.1000 molL1碘的標準溶液滴定。反應原理為:2S2O32-+I2=S4O62-+2I,滴定至終點時,滴定起始和終點的液面位置如下圖,則產品的純度為_____。經儀器分析,該產品純度為16%,分析該興趣小組測定產品純度偏差的原因(忽略人為誤差) 。[M(Na2S2O35H2O)=248g/mol]
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯乙烯是合成聚氯乙烯的單體。乙烯氧化法是生產氯乙烯的主要方法分三步進行。如圖所示:

(1)關于乙烯、氯乙烯、聚氯乙烯說法正確的是____________;
A.都能在氧氣中燃燒 B.都能發生加成反應使溴水褪色
C.都能使得酸性高錳酸鉀褪色 D.氯乙烯分子中所有原子共平面
(2)圖中A物質的化學式為_________;
(3)從環境角度考慮,氧化法的優點是_________;
(4)請寫出③化學方程式_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、W、R是5種短周期元素,其原子序數依次增大。X是周期表中原子半徑最小的元素,Y原子最外層電子數是次外層電子數的3倍,Z、W、R處于同一周期,R與Y處于同一族,Z、W原子的核外電子數之和與Y、R原子的核外電子數之和相等。下列說法正確的是
A. 元素Y、Z、W具有相同電子層結構的離子,其半徑依次增大
B. 元素X只能與元素Y形成一種化合物
C. 元素W、R的最高價氧化物的水化物都是強酸
D. 元素Y、R分別與元素X形成的化合物的熱穩定性![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】固體氧化物燃料電池是由美國西屋(Westinghouse)公司研制開發的。它以固體氧化鋯—氧化釔為電解質,這種固體電解質在高溫下允許氧離子(O2-)在其間通過。該電池的工作原理如下圖所示,其中多孔電極a、b均不參與電極反應。下列判斷正確的是

A. 有O2放電的a極為電池的負極
B. O2-移向電池的正極
C. b極對應的電極反應為2H2-4e-+2O2-=2H2O
D. a極對應的電極反應為O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究表明,化學反應的能量變化與反應物和生成物的鍵能有關。鍵能可以簡單的理解為斷開1mol化學鍵時所需吸收的能量。下表是部分化學鍵的鍵能數據:

己知白磷的燃燒方程式為:P4(s)+ 5O2=P4O10(s),該反應放出熱量2378.0kJ,且白磷分子結構為正四面體,4個磷原子分別位于正四面體的四個頂點,白磷完全燃燒的產物結構如右圖所示,則上表中X 為( )
A.434 B.335 C.237 D.188
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,在2 L的密閉容器中,加入1 mol X(g)和2 mol Y(g)發生反應:X(g)+mY(g)![]() 3Z(g)。平衡時,X、Y、Z的體積分數分別為30%、60%、10%。在此平衡體系中加入1 mol Z(g),再次達到平衡后,X、Y、Z的體積分數不變。下列敘述不正確的是
3Z(g)。平衡時,X、Y、Z的體積分數分別為30%、60%、10%。在此平衡體系中加入1 mol Z(g),再次達到平衡后,X、Y、Z的體積分數不變。下列敘述不正確的是
A.m=2
B.第二次平衡時,Z的濃度為0.4 mol·L-1
C.兩次平衡的平衡常數相同
D.X與Y的平衡轉化率之比為1∶1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】合成氨工業上常用下列方法制備H2:
方法①:C(s)+2H2O(g)![]() CO2(g)+2H2(g)
CO2(g)+2H2(g)
方法②:CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
(1)已知①C(石墨)+O2(g)═CO2(g)△H=-394kJmol-1
②2C(石墨)+O2(g)═2CO2(g)△H=-222kJmol-1
③2H2(g)+O2(g)═2H2O(g)△H=-484kJmol-1
試計算25℃時由方法②制備1000gH2所放出的能量為______kJ。
(2)在一定的條件下,將C(s)和H2O(g)分別加入甲、乙兩個密閉容器,發生反應:C(s)+2H2O(g)![]() CO2(g)+2H2(g)其相關數據如下表所示:
CO2(g)+2H2(g)其相關數據如下表所示:

①T1______T2(填“>”、“=”或“<”);T1℃時,該反應的平衡常數K=______。
②乙容器中,當反應進行到1.5min時,H2O(g)的物質的量濃度范圍是______。
③在密閉恒容的容器中,能表示上述反應達到化學平衡狀態的是______。
A.V逆CO2)=2V正H2)
B.混合氣體的密度保持不變
C.c(H2O):c(CO2):c(H2)=2:1:2
D.混合氣體的平均摩爾質量保持不變
④某同學為了研究反應條件對化學平衡的影響,測得逆反應速率與時間的關系如圖所示:

在t1、t3、t5、t7時反應都達了到平衡狀態,如果t2、t4、t6、t8時都只改變了一個反應條件,則t6時刻改變的條件是________________________,從t1到t8哪個時間段H2O(g)的平衡轉化率最低______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從廢電池外殼中回收鋅(鋅皮中常有少量鐵、外表沾有NH4Cl、ZnCl2、MnO2等雜質),制取ZnSO4·7H2O可以采取如下工藝流程:

金屬氫氧化物沉淀的pH:
氫氧化物 | 開始沉淀的pH | 完全沉淀的pH |
Zn(OH)2 | 5.7 | 8.0 |
Fe(OH)3 | 2.7 | 3.7 |
![]() 回答下列問題:
回答下列問題:
(1)酸溶時常常加入少量的CuSO4,其目的是 。
(2)寫出氧化時的離子方程式 。該過程中加入的H2O2量要遠多于理論值,原因除了提高另外反應物的轉化率外,還可能是 。
(3)調節pH大于8后會造成鋅元素轉化率降低,其原因是 。
(4)從濾液B獲得Na2SO4應該采用的方法是蒸發結晶, ,洗滌干燥。(部分物質的溶解度曲線見下圖)

(5)由濾渣B制備ZnSO4·7H2O的實驗方案為:_ __ __,干燥得到ZnSO4·7H2O (實驗中須使用的試劑有:1mol/LH2SO4,蒸餾水,乙醇;除常用儀器外須使用的儀器有:pH計)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com