
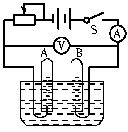
圖為電解水的實驗裝置,閉合開關S后,觀察到電壓表的示數為6.0V,電流表的示數為100mA。
(1)此時A管內生成_____氣,B管內生成_____氣。
(2)試寫出電解水的總反應式:_____________。
(3)通電過程中,A極、B極各發生何種電極反應:_______________。
(4)為了加快電解水的速率,可在水中加入_____。
A.H2SO4 B.HCl C.NaOH D.NaCl
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:閱讀理解

查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
 化工中把電解飽和食鹽水的工業生產叫氯堿工業,其生產流程如下:
化工中把電解飽和食鹽水的工業生產叫氯堿工業,其生產流程如下: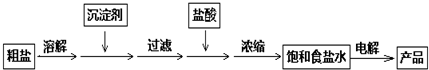
查看答案和解析>>
科目:高中化學 來源: 題型:

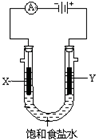
(1)此時A管內生成____________氣,B管內生成____________氣。
(2)試寫出電解水的化學方程式。
(3)通電過程中,A極、B極各發生何種化學反應?
(4)為了加快電解水的速率,可在水中加入_____________________________。
A.H2SO4 B.HCl C.NaOH D.NaCl
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com